Situação de Aprendizagem 4 – Utilizando a grandeza quantidade de matéria (mol); concentração em mol . L-1. Fazer usos da linguagem química; construir o conceito de concentração em quantidade de matéria/volume para ampliar a compreensão do significado da concentração e aplica-lo a novas situações que permitem melhor entendimento do mundo físico.
CONTEÚDOS E TEMAS: Relações quantitativas de massa e de quantidade de matéria (mol) nas transformações químicas que ocorrem em soluções.
COMPETÊNCIA E HABILIDADES.Construir e aplicar conceitos relativos ás proporções de reagentes e produtos numa reação em solução, compreendendo a importância desses cálculos na sociedade; interpretar a equações químicas em termos quantitativos.
5. Concentração em mol/L Molaridade (M)
A molaridade de uma solução é a concentração em número de mols de soluto e o volumede 1L de solução.Onde:
M = molaridade (mol/L)
n1= número de mols do soluto (mol)
V = volume da solução (L)Concentração é o termo que utilizamos para fazer a relação entre a quantidade de soluto e a quantidade de solvente em uma solução.
As quantidades podem ser dadas em massa, volume, mol, etc.
Observe:
m1= 2g
n2 = 0,5mol
V = 14L
Exemplos:
massa de 2g do soluto NaCl: m1= 2g
número de mols de 0,5mol do solvente água: n2 = 0,5mol
volume da solução de 14L:
V = 14L
Em laboratório, é muito importante conhecer a concentração em mol/L das soluções químicas
A concentração em mol/L (M) é também muito conhecida como Concentração Molar, e também Molaridade. No entanto, esses nomes, apesar de bastante difundidos, não são recomendados pela SBQ (Sociedade Brasileira de Química).
Os nomes corretos são Concentração em mol/L ou Concentração em quantidade de matéria.Em laboratórios e indústrias químicas, essa é a concentração mais utilizada, pois é a recomendada pelo Sistema Internacional de Unidades (SI) e pela União Internacional da Química Pura e Aplicada (IUPAC).
É uma relação mais sofisticada que a concentração comum.Seu cálculo é feito dividindo-se a quantidade de matéria ou substância (mol) pelo volume da solução, conforme a expressão matemática abaixo:
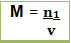
Onde M = concentração em mol/L
n1 = número de mols do soluto (mol), lembrando que o índice 1 indica grandezas relacionadas ao soluto
v = volume da solução (L)Desse modo, se for dito que uma solução tem concentração de 4,5 mol/L, quer dizer que em cada litro da solução (não do solvente) tem-se dissolvidos 4,5 mols do soluto.
Porém, em laboratório é mais fácil conseguir a massa em gramas do soluto e a sua massa molar, do que a sua quantidade de máteria em mols.
Assim, sabendo-se que: 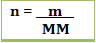 ou se referindo ao soluto:
ou se referindo ao soluto:
Podemos substituir o valor de n1 na fórmula da concentração em mol/L e teremos:

Considere o problema abaixo para ver como se usa essa fórmula a fim de determinar a concentração de uma solução:“Qual será a concentração em quantidade de matéria de uma solução que foi preparada dissolvendo-se 120 g de hidróxido de sódio em 2 L de água e obteve-se uma solução com 2 L?”Dados:
m1 = 120 g
v = 2 L
MM (NaOH) = 40 g/mol• Substituindo os valores dados na fórmula:
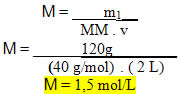
(UFV – MG) Uma solução aquosa de ácido sulfúrico (H2SO4) de densidade 1,2g/mL, foi formada pela reunião de 24,5g de ácido sulfúrico e 275,5g de água.
Dados: MM1 = 98g/mol
Determine:
a) a massa é o número de mols de soluto
GABARITO: o ácido sulfúrico é o soluto, logo sua massa é de 24,5g
98g ————– 1 mol X = 0,25 mol de H2SO4
24,5g ————– X
b) o volume da solução, em litros
GABARITO: d = 1,2 g/ml
M = 275,5 + 24,5 = 300g
1,2g ————— 1 ml Y = 250 ml = 0,25 L
300g ————– Y
(ESCS – DF) Uma solução tem 230g de álcool comum (CH3CH2OH) e 360g de água. As frações molares do álcool e da água na solução são, respectivamente:
a) 0,6 e 0, 8
b) 0,8 e 0,2
c) 0,8 e 0,6
d) 0,2 e 0,6
e) 0,2 e 0,8
GABARITO: LETRA “E”
Como nessa prova a tabela periódica é fornecida, temos que a massa de CH3CH2OH é igual a 46g/mol e a massa de água é de 18g/mol. Temos agora que:
. do álcool: n1 = m1 = 230 = 5 mols
M1 46
. da água: n1 = m1 = 360 = 20 mols
M1 18
Total: 5 + 20 = 25 mols
Frações molares:
. X1 = __ n1________
n1 + n2
. álcool: X1 = __ _5______ = 0,2
5 + 20
.água: X1 = __ 20________ = 0,8
5 + 20
Note que: 0,2 + 0,8 = 1
https://www.youtube.com/watch?v=D4fEHBYT7Kc


