Conteúdos e temas: separação de misturas.
Competências e habilidades: compreender os processos de separação das misturas ferro/escória no alto-forno e água/álcool aplicando as propriedades específicas estudadas na Situação de Aprendizagem 5.
Sugestão de estratégias de ensino: leituras de textos orientadas por perguntas; pesquisa orientada e apresentações.
Avaliação: respostas às perguntas e apresentação oral e escrita da pesquisa.
A NECESSIDADE DE SEPARAR MISTURAS E SUA IMPORTÂNCIA PARA O SISTEMA PRODUTIVO.
Substâncias e Misturas
A água destilada é formada só por H2O, sendo uma substância pura. Porém, outros “tipos de água” são misturas porque possuem substâncias dissolvidas
No cotidiano nos referimos a muitos compostos utilizando a palavra “substância”. No entanto, será que estamos fazendo o uso correto dessa palavra? Em química, o que significa “substância”?
Substância química é qualquer espécie de matéria formada por uma composição constante de elementos químicos, e que tenha propriedades físicas e específicas definidas.
Por exemplo, a água destilada é uma substância, pois ela é constituída unicamente de água, ou seja, H2O, e suas propriedades físicas, tais como o ponto de fusão, o ponto de ebulição e a densidade, são bem definidas, conforme mostrado nos dados abaixo, ao nível do mar (1 atm):
PF = 0 ºC
PE = 100 ºC
d = 1,0 g/cm3 a 3,98ºC
A água é um exemplo de substância composta, ou seja, é formada por moléculas com mais de um tipo de elemento. Mas também existem substâncias simples, como o gás oxigênio (O2), que é formado por apenas um tipo de elemento.
Não existem duas substâncias que tenham todas as propriedades exatamente iguais. Veja mais alguns exemplos de substâncias: álcool etílico anidro (sem água), gás carbônico, cloreto de sódio, mercúrio, iodo, ouro, silício, gás nitrogênio, gás hélio e ferro.
Mas não é correto nos referirmos à água da chuva, do mar, à água mineral, da torneira, à água potável ou de um rio como sendo substâncias. Na realidade essas águas possuem outras substâncias dissolvidas nelas. Por exemplo, a água do mar contém vários sais, como o sal de cozinha (cloreto de sódio – NaCl), que pode ser extraído dela por evaporação e cristalização.
O correto seria dizermos que elas são misturas.
A fusão e a ebulição das misturas ocorrem em determinada faixa de temperatura e apresentam densidades diferentes em função de sua composição.
TIPOS DE MISTURA
Em nosso dia-a-dia é dificílimo encontrarmos substâncias puras na natureza. Em sua grande maioria, as substâncias aparecem em misturas.
Chama-se mistura a união física de duas ou mais substâncias, e a maior parte delas pode ser separada por métodos físicos.
Há dois tipos de mistura.
As misturas podem ser classificadas em homogêneas e heterogêneas de acordo com seu aspecto visual.
Mistura homogênea ou solução: é aquela cujos componentes (soluto e solvente) não se distinguem visualmente, ou seja, ela apresenta uma única fase, que tem as mesmas propriedades por toda a sua extensão. Por exemplo: ar atmosférico filtrado, ligas metálicas e água potável.
Mistura heterogênea: é aquela cujos componentes (soluto e solvente) apresenta mais de uma fase, podem se distinguir visualmente. Por exemplo: granito, concreto, mistura de farinha e água, água e óleo, água e areia.
Por exemplo, o álcool hidratado tem a sua densidade variando de acordo com a porcentagem de álcool etílico e de água que constitui a mistura.
O álcool hidratado é uma mistura homogênea ou solução, pois apresenta uma única fase. Outros exemplos de misturas homogêneas são o soro caseiro, o soro fisiológico, a gasolina, o vinagre etc.
No entanto, quando a mistura apresenta mais de uma fase, como, por exemplo, uma mistura de areia e água, dizemos que é uma mistura heterogênea. Também são misturas heterogêneas: quartzo, água e óleo, a própria areia, a madeira, o sangue, o leite, água com gás, entre outros.
Talvez você esteja se perguntando: mas, o leite e o sangue são homogêneos?! Na realidade, eles parecem ter uma única fase a olho nu; porém, os cientistas basearam esse conceito em dois aparelhos sofisticados: o ultramicroscópio e a ultracentrífuga.
Se usarmos um ultramicroscópio para visualizar o álcool hidratado e o sangue, observaremos que o álcool hidratado é totalmente uniforme, enquanto que o sangue apresenta aspecto desigual, sendo, portanto, constituído de mais de uma fase. Além disso, se usarmos uma ultracentrífuga, veremos que haverá uma separação no caso do sangue, como mostra a imagem a seguir:
Na natureza, a grande maioria são misturas e não substâncias.
Soluto
Todo componente minoritário em uma solução.
Solvente
Componente que está em maior quantidade em uma solução.
Fase
Porção de um sistema que apresenta as mesmas propriedades em toda a sua extensão.
Liga
Mistura homogênea de duas ou mais substâncias, sendo pelo menos uma delas um metal.
SEPARAÇÃO DE MISTURAS
A separação das misturas é baseada nas propriedades de cada substância.
Até agora, você estudou três propriedades físicas importantes: a densidade, a temperatura de fusão e a de ebulição. Como elas poderiam ser utiliza- das para separar a mistura de areia, casca- lho, cortiça e sal seus componentes tiverem propriedades diferentes.
Todo processo de separação tem uma lógica associada a característica daquela substância a ser retirada.
São eles:
Catação: separação manual de sólidos diferentes.

Centrifugação: através da utilização de uma centrifuga, que agiliza a decantação.A centrifugação separa substâncias com densidades diferentes. Ao contrário da decantação que deixa o líquido em repouso, descansando, a centrifugação faz girar a mistura em uma centrífuga e acelera o processo de separação dos elementos mais densos, que tendem a se deslocar na direção de fuga. Com isso é possível separar as partículas mais densas.

A centrifugação é usada nos diversos ramos da indústria e neste vídeo abaixo te mostro uma aplicação prática deste assunto, o chamado Hidrociclones.
Espere você entende espanhol, mas apesar disso, achei o vídeo muito interessante e fácil de entender. Dá uma olhadinha nele para você entender como a centrifugação é um processo de separação de misturas.
http://www.youtube.com/watch?v=tLA6w9L4JXE
Cristalização – Processo de Separação de Misturas
A cristalização é o processo de separação de misturas na qual é fornecido calor para uma solução com intuito de evaporar o solvente e concentrar o soluto até ele cristalizar-se.
Este é o processo utilizado para obtenção do nosso sal de cozinha, que você adiciona nos alimentos.
Veja esse vídeo abaixo para você ver a aplicação prática do processo de cristalização.
Decantação: quando houver substâncias com diferentes densidades. Uma delas se deposita no fundo do recipiente e pode ser retirada.

As substâncias mais densas (pesadas) tenderão a se depositar no fundo do recipiente, enquanto as substâncias menos densas (leves), tenderão flutuar, subir. Essa é a ideia da decantação. Após essa separação das substâncias por conta de sua densidade, fica mais fácil de separamos cada uma.
É o caso da separação de água e óleo, separação de misturas de plásticos, limpeza de água turva.

Se você pega uma mistura de água e óleo e deixar ela paradinha, descansando, o óleo vai flutuar na água, enquanto a água vai ser depositada em baixo. O mesmo acontece com a água turva. Pegue uma água barrenta e deixe-a descansar para ver o que acontece. Com o tempo os sólidos dispersos vão decantar, descer para o fundo do recipiente.
O processo de decantação consiste, portanto, em deixar em repouso (“descansar”) a mistura, para que as substâncias mais densas se separem das demais e se depositem no fundo do recipiente.
Destilação simples: quando há temperaturas de ebulição distintas.
Destilação fracionada: semelhante à destilação simples, mas no vidro há diversos obstáculos que retém as partes da mistura aos poucos.
Destilação – Processo de Separação de Misturas
A destilação é o processo de separação de misturas que utiliza a volatilidade das substâncias para fazer a separação através do fornecimento de calor. Neste processo, o calor faz um líquido evaporar. Em sequência, o vapor passa por um processo de condensação onde é transformado em líquido novamente, só que dessa vez, com maior grau de pureza.

O processo de Destilação é muito comum para separar líquido de soluto não volátil. Exemplo solução de água e sal. Se você tem uma solução de água e sal, e aquece essa solução, a água vai evaporar enquanto o sal vai continuar no recipiente. Com o tempo terá separado a água do sal. Após o processo será obtida a água destilada e o sal dentro do recipiente. Entendeu?
Um exemplo prático do processo de destilação é o que acontece no processo de fabricação de álcool (etanol). Na indústria sucroalcooleira, após a etapa de fermentação, a mistura formada por água, álcool e outros compostos passa pelo processo de destilação, no qual se consegue separar o álcool (mais volátil) da mistura, e condensá-lo, obtendo o álcool etanol que conhecemos.
Para você conhecer um pouco mais sobre essa aplicação, assista ao vídeo abaixo:

Destilação Fracionada – Processo de Separação de Misturas
A destilação fracionada também utiliza calor para evaporar substâncias e separá-las das demais. A diferença da destilação simples é que neste caso, tem-se uma mistura de substâncias líquidas com pontos de ebulição diferentes. A separação é feita de forma fracionada, tal que, as substâncias de menor ponto de ebulição são separadas primeiro, em seguida, separa-se a substância de maior ponto de ebulição e assim sucessivamente.
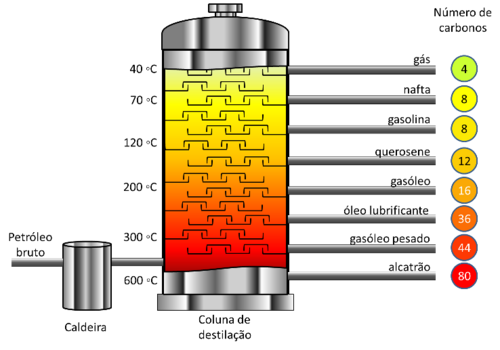
Na prática, o processo de destilação fracionada é feita na separação dos constituintes do petróleo.
Dissolução fracionada: pode ser utilizada quando um dos componentes da misture é solúvel em líquido. Depois de dissolvida uma das partes, a outra é filtrada e o restante evaporado.Veja esse vídeo do Manual do Mundo, em que se faz um teste de adulteração de gasolina. Perceba que após misturar, água, gasolina e álcool, houve uma separação entre os líquidos imiscíveis graças a diferença de densidade entre eles. A gasolina além de não se misturar a àgua, possui menor densidade, concentrando-se na parte superior do recipiente.
Filtração é um processo físico de separação de misturas heterogêneas sólido – líquido ou sólido – gasoso, que consiste basicamente em passar a mistura de interesse através de um meio filtrante que é alocado em um funil de vidro (no caso de filtrações em pequena escala, feitas em laboratório), onde a fração sólida da mistura fica retida no meio filtrante, formando o que chamamos de torta, e a fração líquida ou gasosa, chamada de filtrado.
A separação de um sólido insolúvel a partir um líquido se dá, de melhor forma, por meio da filtração. O método é muito utilizado no cotidiano durante a preparação do café, por exemplo, ou ainda para a remoção de substâncias sólidas nas estações onde ocorre o tratamento da água potável.

Tipos de filtração
Existem dois tipos observados de filtração, a filtração simples (ou também chamada de comum) e a filtração a vácuo. Ambas apresentam características pontuais e podem ser explicada a partir de etapas claras da separação das substâncias.
Filtração simples ou comum
A filtração simples ocorre de modo que a inserção de uma barreira, tal como o filtro de papel ao coar o café, promova a separação de substâncias. Dessa maneira, o filtro anexado na entrada do recipiente, e a mistura do líquido (água quente) e pó de café permanece no filtro.
As partículas sólidas (o pó), que também recebe denominação de resíduo, permanece no filtro/barreira, separada do material filtrado, no caso o café coado.
Filtro a vácuo
A filtração a vácuo exige um pouco mais de tato para definição do que a filtração simples ou comum. Também denominada por filtração de pressão reduzida, tem como utilização o aceleramento no processo de separação, abrangendo a rarefação do ar abaixo do recipiente a filtrar.

O processo ocorre, comumente, no que denomina-se funil de Buchner – instrumento em porcelana com furo ao fundo. O funil em questão é colocado sobreposto ao kitassato, recebendo o líquido a ser filtrado.
Esse processo é muito mais dispendioso, visto que é uma técnica utilizada que separa um produto solidificado por meio de uma substância líquida solvente através de reação química.
No processo, portanto, a mistura do sólido e do líquido é vertida por meio de um papel alocado em um funil de Buchner. Dessa maneira o sólido se prende ao filtro, o líquido é retirado por meio do funil através do balão e todo o processo é feito através do vácuo gerado.
Floculação – Processo de Separação de Misturas
Floculação é o processo de separação de misturas em que se formam flocos com o intuito de aumentar a densidade e fazê-lo depositar no fundo do recipiente.

Como isso é feito? A floculação geralmente segue o processo de coagulação em que uma substância química, chamada de coagulante, é adicionada à mistura para que formem coágulos das partículas suspensas. Na etapa de floculação há uma aglutinação desses coágulos se transformando em flocos com maior densidade, que após decantação, sofrem uma deposição, sendo possível sua separação.
A floculação é etapa importante no processo de tratamento da água. Dá uma olhadinha neste vídeo sobre tratamento da água.
Processo de Separação de Misturas modernos
Um moderno processo de separação de misturas muito discutido como alternativa de solução para o problema da seca e fornecimento de água potável em vários países é o processo de Dessalinização de água do mar através da Osmose Reversa. Assista ao vídeo abaixo para conhecer mais sobre este processo.
Peneiração: usada entre dois sólidos de tamanhos diferentes. Exemplo: Pedra e areia.

Levigação: usada entre sólidos heterogêneos através da mistura de um deles à água. Este processo é utilizado nos garimpos onde o garimpeiro com uma peneira procura o ouro no fundo dos rios.

Flotação: usada para separar sólidos de densidade diferentes. Enquanto um deles afunda, o outro permanece na superfície.
Fusão fracionada: quando as substâncias químicas possuem pontos de fusão diferenciados, uma delas é aquecida e separada.
Sublimação: é a passagem de solido para gás que algumas substâncias químicas podem sofrer, com o aquecimento adequado.
Levigação é um processo de separação de misturas heterogêneas de sólidos, com outras palavras, quando se tem dois sólidos de diferentes densidades onde se quer separar um do outro utilizando a levigação.
Separação magnética é útil para separar misturas heterogêneas, onde um dos componentes da mistura é atraído por um ímã ou um eletroímã.
Sifonação é o processo de transporte de um líquido de um nível mais alto a outro mais baixo. O sifão funciona sugando o líquido para o seu interior.
O que ocorre é que a coluna de líquido na parte baixa do sifão é mais longa. Ela é maior que a coluna na parte alta. E seu peso é maior. Além de ser um método de separação de substâncias líquidas em laboratório, há outras aplicações no dia-a-dia, pois, por exemplo, é o processo que ocorre quando se usa uma mangueira para retirar combustível do tanque de um automóvel: a pessoa coloca a mangueira no tanque, suga até que o combustível venha até a saída da mangueira e, colocando esta extremidade abaixo do nível do tanque, o combustível vai sendo extraído.
Exercícios Sobre Separação
Questão 1
Um estudante de Química precisou fazer uma destilação simples de uma mistura formada por sulfato de cobre penta-hidratado e água. Para atingir seu objetivo, ele utilizou diversos equipamentos, entre os quais estava um
- a) condensador.
- b) funil de Buchner.
- c) balão volumétrico.
- d) kitassato.
- e) filtro de papel.
Questão 2
Os equipamentos da imagem a seguir são usados no método de separação de misturas denominado destilação simples:
Nesse método, ocorrem duas transformações de estado físico: uma do líquido para o gasoso, e a outra do gasoso para o líquido. Assinale a alternativa que apresenta, respectivamente, o nome dos equipamentos em que essas mudanças acontecem:
- a) Balão de destilação e erlenmeyer.
- b) Condensador e erlenmeyer.
- c) Balão de destilação e condensador.
- d) Condensador e erlenmeyer.
- e) Condensador e balão de destilação.
Questão 3
(UFU-MG) A destilação também era utilizada em manufaturas, como na preparação de perfumes, artes para a qual os árabes muito contribuíram. Havia grandes centros onde eram extraídos os aromas de rosas, violetas, jasmins e de outros materiais. Para isso, as flores eram maceradas em água e, em seguida, esse material era destilado. Tal processo não era utilizado na Antiguidade, predominando então o método de extração de essências pela infusão de flores em óleos ou gorduras.
BELTRAN, M.H.R. Destilação: a arte de extrair virtudes.
Revista Química Nova na Escola, nº 4, novembro, 1996, p. 26.
Imagem representando o processo de destilação,
extraída da obra de Hieronymus Brunschwig (Liber de arte distillandi, 1512).
A destilação, incorporada como um procedimento químico no século XVIII,
- a) era utilizada, na antiguidade, como principal método de extração das essências após se fazer uma mistura heterogênea.
- b) é uma técnica ideal para extração de essências de rosas que, ao serem maceradas, tornam-se sistemas homogêneos com a água.
- c) é uma técnica de separação que requer aquecimento da mistura homogênea ao longo do procedimento.
- d) possui uma etapa de resfriamento e, em seguida, de condensação da água onde estarão dissolvidas essências oleosas.
Questão 4
(UFSM-RS) A vitamina C é importante para o nosso cérebro, pois tem ação antioxidante. Ela contém vários grupos hidroxila, por isso é solúvel em água. Em um laboratório, ao serem realizados alguns testes, comprimidos contendo vitamina C são dissolvidos em água suficiente para formar uma solução homogênea. Esse sistema, uma vez formado, será separado posteriormente, através de:
a) destilação fracionada.
b) sublimação.
c) destilação simples.
d) decantação.
e) filtração.
Questão 5
Analise cada uma das afirmativas feitas sobre os quatro sistemas propostos a seguir:
- água e gasolina
- metanal (CH2O)
- nitrogênio (N2)
- água e metanol
1) Os sistemas I, II, III e IV são, respectivamente, mistura heterogênea, substância composta, substância simples e mistura homogênea.
2) Para realizar a separação dos componentes do sistema I, deve-se usar o processo de destilação fracionada.
3) Se misturarmos os componentes do sistema I e IV, haverá uma mistura heterogênea trifásica.
4) Para realizar a separação de cada um dos componentes do sistema IV, deve-se usar o processo de destilação fracionada.
5) A mistura formada pelos sistemas II e III pode ser separada por decantação.
As afirmações que estão corretas são:
- a) 1, 2, 4
- b) 1, 2, 3
- c) 2, 3, 5
- d) 3, 4, 5
- e) 1, 3 e 4
QUESTÃO 6
Sabe-se que o petróleo é formado pela mistura de diversas substâncias químicas diferentes, as quais são separadas umas das outras por meio do(a):
- a) Filtração a vácuo
- b) Destilação simples
- c) Decantação
- d) Destilação fracionada
QUESTÃO 7
(Enem) O principal processo industrial utilizado na produção de fenol é a oxidação do cumeno (isopropilbenzeno). A equação mostra que esse processo envolve a formação do hidroperóxido de cumila, que em seguida é decomposto em fenol e acetona, ambos usados na indústria química como precursores de moléculas mais complexas. Após o processo de síntese, esses dois insumos devem ser separados para comercialização individual.

Considerando as características físico-químicas dos dois insumos formados, o método utilizado para a separação da mistura, em escala industrial, é a:
- a) filtração
- b) ventilação.
- c) decantação.
- d) evaporação.
- e) destilação fracionada.
QUESTÃO 8
(Asces-PE) Um erlenmeyer contém um sistema heterogêneo bifásico formado por água, acetona e tetracloreto de carbono. Sabendo que acetona e água são miscíveis entre si, que o tetracloreto de carbono é imiscível em água e em acetona, e que a acetona é um líquido mais volátil que a água, assinale os métodos mais adequados para separar esses três líquidos.
- a) Decantação e fusão fracionada.
- b) Filtração e decantação.
- c) Centrifugação e decantação.
- d) Decantação e destilação fracionada.
- e) Filtração e destilação fracionada.
Resposta Questão 1
Letra a). Dos materiais indicados nas alternativas, o único utilizado em uma destilação é o condensador.
b- O funil de Buchner é utilizado na filtração a vácuo.
c- O balão volumétrico é usado para realizar a medida de um volume específico de um líquido.
d- Kitassato é utilizado na filtração a vácuo.
e- Filtro de papel é utilizado na filtração.
Resposta Questão 2
Letra c). Na destilação simples, ocorre a separação dos componentes de uma mistura homogênea formada por um sólido e um líquido. Inicialmente, essa mistura é colocada no balão de destilação para sofrer um aquecimento e o líquido ser transformado em gás.
Em seguida, o gás sai do interior do balão de destilação e desloca-se no sentido do condensador, onde o gás será transformado em líquido novamente.
Resposta Questão 3
Letra c). A destilação tem como ponto inicial o aquecimento de uma mistura homogênea.
a- Refere-se ao método utilizado em misturas homogêneas.
b- As rosas maceradas com água formam um sistema heterogêneo.
d- O método baseia-se em aquecimento e, em seguida, na condensação do material vaporizado.
Resposta Questão 4
Letra c). O único método capaz de separar os componentes de uma mistura homogênea, formada por um sólido e um líquido, é a destilação simples. Em relação aos outros métodos mencionados:
a- É utilizado em mistura homogênea formada por líquidos.
b- É utilizado em mistura homogênea formada por sólidos.
d- É utilizado em misturas heterogêneas formadas por líquidos ou por sólido e líquido.
e- É utilizado em misturas heterogêneas formados por sólido e líquido ou sólido e gás.
Questão 5
Letra e). As afirmações 2 e 5 estão incorretas porque:
2- Água e gasolina não são miscíveis (não se dissolvem), logo, para separá-las, devemos utilizar o método da decantação;
5- A mistura formada pelos sistemas II e V só pode ser separada por destilação fracionada, pois o metanal é uma substância polar, assim como a água e o metanol, logo, são todos miscíveis (dissolvem-se).
Questão 6
Letra d). Como o petróleo é uma mistura homogênea formada por diversos líquidos dissolvidos, o método mais apropriado para fazer a separação de seus componentes é a destilação fracionada.
Questão 7
Letra e). Para separar fenol e acetona, usa-se a destilação fracionada, pois a mistura é homogênea e formada por líquidos miscíveis. Eles são miscíveis porque são polares, já que o fenol apresenta um grupo bastante eletronegativo (OH), e a acetona, um átomo bastante eletronegativo (oxigênio) em uma cadeia carbônica pequena.
Questão 8
Letra d). A mistura fornecida pelo exercício é bifásica e formada por três líquidos. O tetracloreto forma uma fase, e a água e a acetona formam outra. Assim sendo, inicialmente se realiza a decantação para separar o tetracloreto de carbono, já que ele não é miscível aos outros líquidos; depois, para separar a água da acetona, que é uma mistura homogênea, devemos utilizar a destilação fracionada.
(UFSM-RS) A vitamina C é importante para o nosso cérebro, pois tem ação antioxidante. Ela contém vários grupos hidroxila, por isso, é solúvel em água. Em um laboratório, ao serem realizados alguns testes, comprimidos contendo vitamina C são dissolvidos em água suficiente para formar uma solução homogênea. Esse sistema, uma vez formado, será separado posteriormente por meio de:
- a) destilação fracionada.
- b) sublimação.
- c) destilação simples.
- d) decantação.
- e) filtração.
QUESTÃO 2
(UFU-MG) Sobre os procedimentos químicos da destilação de uma solução aquosa de sal de cozinha e suas aplicações, assinale a alternativa correta.
- a) O sal de cozinha entra em ebulição ao mesmo tempo que a água e é colhido no erlenmeyer.
- b) O condensador possui a função de diminuir a temperatura dos vapores produzidos pelo aquecimento e, assim, liquefazer a água.
- c) A temperatura de ebulição do sal de cozinha é menor que a temperatura de ebulição da água.
- d) A eficiência do método de destilação é pequena para separar o sal da água.
QUESTÃO 3
A representação esquemática a seguir do método de separação denominado destilação simples:
Sabe-se que esse método deve ser utilizado quando uma mistura for homogênea e apresentar um ou mais sólidos dissolvidos em um líquido. Assim, qual das misturas propostas abaixo poderia ser separada por esse método de separação?
- a) Petróleo
- b) Água e dissulfeto de carbono
- c) Água e nitrato de sódio
- d) Água e acetona
- e) Água e sulfato de cálcio
QUESTÃO 4
“O ciclo da água, também chamado por ciclo hidrológico, ocorre por meio das mudanças dos estados físicos e da movimentação dessa substância pelos seres vivos e meio ambiente. Esse ciclo depende diretamente da energia solar, dos movimentos de rotação da Terra e até mesmo da gravidade. O Sol é o responsável por levar energia para que o ciclo aconteça. Sua luz provoca a evaporação da água presente na superfície terrestre. Essa água, agora em estado gasoso, sobe para camadas mais altas da atmosfera, onde a temperatura é mais baixa. Ao alcançar determinada altitude, a água passa do estado de vapor para o líquido (condensação) e forma as nuvens, que são, na realidade, uma grande quantidade de gotículas de água. Em locais extremamente frios, essas gotículas podem solidificar-se e dar origem à neve ou ao granizo.”
A partir do exposto no texto acima, as transformações de estados físicos da água que ocorrem no ciclo hidrológico, assemelham-se ao que ocorre em qual método de separação de misturas?
- a) Ao método de destilação.
- b) Ao método de catação.
- c) Ao método de filtração.
- d) Ao método de decantação.
- e) Ao método de peneiração.
RESPOSTAS
Questão 1
Letra c). A mistura entre o comprimido de vitamina C e água é caracterizada por ser uma mistura homogênea composta por um sólido dissolvido em um líquido, característica fundamental para a realização de uma destilação simples. As outras alternativas estão incorretas porque:
- a) É um método utilizado para separar misturas homogêneas formadas por líquidos.
- b) É um método utilizado para separar misturas homogêneas formadas por sólidos, em que um deles é sublimável.
- d) É um método utilizado para separar misturas heterogêneas formadas por dois ou mais líquidos, ou entre um sólido e um líquido.
- e) É um método utilizado para separar mistura heterogênea formada por sólido e líquido.
Questão 2
Letra b). As outras alternativas estão incorretas porque:
- a) O ponto de ebulição de substâncias é o mesmo apenas no caso de misturas azeotrópicas, que são aquelas misturas homogêneas formadas por quantidades específicas de líquidos diferentes.
- c) Por ser uma substância iônica, o sal de cozinha (cloreto de sódio, NaCl) apresenta um ponto de ebulição maior que a água, que é uma substância molecular.
- d) Por ser homogênea, formada por sólido dissolvido em líquido, a mistura sal e água deve ser separada por destilação simples.
Questão 3
Letra c). Na alternativa c, temos a presença de uma mistura homogênea formada por um sólido dissolvido em um líquido, característica fundamental para a utilização da destilação simples. As outras alternativas estão erradas porque:
- a) É uma mistura homogênea formada por diversos líquidos miscíveis (que são solúveis entre si), logo, deve ser separada por destilação fracionada.
- b) É uma mistura heterogênea formada por dois líquidos imiscíveis (pois o dissulfeto de carbono é insolúvel em água), logo, deve ser separada por decantação no funil de separação.
- d) É uma mistura homogênea formada por dois líquidos, logo, deve ser separada por destilação fracionada.
- e) É uma mistura heterogênea (pois o sulfato de cálcio é praticamente insolúvel em água), formada por um sólido e um líquido, logo, deve ser separada por filtração.
Questão 4
Letra a). No ciclo hidrológico, a água passa pelas transformações de estados físicos denominadas vaporização e condensação, o que também ocorre apenas na destilação.
Exercícios com Gabarito de Química Separação de Fases
1) (VUNESP-2006) A preparação de um chá utilizando os já tradicionais saquinhos envolve, em ordem de acontecimento, os seguintes processos:
- A) filtração e dissolução.
- B) filtração e extração.
- C) extração e filtração.
- D) extração e decantação.
- E) dissolução e decantação.
2) (Vunesp-2005) A água potável é um recurso natural considerado escasso em diversas regiões do nosso planeta. Mesmo em locais onde a água é relativamente abundante, às vezes é necessário submetê-la a algum tipo de tratamento antes de distribuí-la para consumo humano. O tratamento pode, além de outros processos, envolver as seguintes etapas:
- manter a água em repouso por um tempo adequado, para a deposição, no fundo do recipiente, do material em suspensão mecânica.
- remoção das partículas menores, em suspensão, não separáveis pelo processo descrito na etapa I.
III. evaporação e condensação da água, para diminuição da concentração de sais (no caso de água salobra ou do mar). Neste caso, pode ser necessária a adição de quantidade conveniente de sais minerais após o processo.
Às etapas I, II e III correspondem, respectivamente, os processos de separação denominados.
- A) filtração, decantação e dissolução.
- B) destilação, filtração e decantação.
- C) decantação, filtração e dissolução.
- D) decantação, filtração e destilação.
- E) filtração, destilação e dissolução.
3) (Vunesp-2003) Uma das formas utilizadas na adulteração da gasolina consiste em adicionar a este combustível solventes orgânicos que formem misturas homogêneas, como o álcool combustível. Considere os seguintes sistemas, constituídos por quantidades iguais de:
1 — gás oxigênio, gás carbônico e gás argônio;
2 — água líquida, clorofórmio e sulfato de cálcio;
3 — n-heptano, benzeno e gasolina; todos nas condições normais de temperatura e pressão.
- a) Indique o número de fases dos sistemas 1, 2 e 3 e classifique-os como sistema homogêneo ou heterogêneo.
- b) Se fosse adicionado querosene ao sistema 3, quantas fases este apresentaria? Justifique sua resposta.
4) (Vunesp-2001) O magnésio pode ser obtido da água do mar. A etapa inicial deste processo envolve o tratamento da água do mar com óxido de cálcio. Nesta etapa, o magnésio é precipitado na forma de:
- a) MgCl2.
- b) Mg(OH)2.
- c) MgO.
- d) MgSO4.
- e) Mg metálico.
5) (Vunesp-1999) Um sistema heterogêneo, S, é constituído por uma solução colorida e um sólido branco. O sistema foi submetido ao seguinte esquema de separação . Ao se destilar o líquido W, sob pressão constante de 1 atmosfera, verifica-se que sua temperatura de ebulição variou entre 80 e 100 °C.
Indique qual das seguintes afirmações é correta:
- a) A operação I é uma destilação simples.
- b) A operação II é uma decantação.
- c) O líquido colorido Y é uma substância pura.
- d) O líquido incolor W é uma substância pura.
- e) O sistema heterogêneo S tem, no mínimo, 4 componentes.
6) (Unirio-1999) “Uma blitz de fiscais da ANP (Agência Nacional de Petróleo) (…) interditou 19 postos de combustíveis em São Paulo (…),14 deles por venda de gasolina adulterada.” JB, 09/09/98 A gasolina, composta basicamente por uma mistura de alcanos na faixa de C6 a C12‚ átomos de carbono, pode ser facilmente adulterada com substâncias mais baratas do que ela. De acordo com a regra de que “semelhante dissolve semelhante”, assinale a opção que contém a única substância que, ao ser adicionada à gasolina, irá formar uma mistura heterogênea.
- A) Água.
- B) Hexanol.
- C) Hexano.
- D) Benzeno.
- E) 2-decanona.
7) (Unifesp-2005) As solubilidades dos sais KNO3 e NaCl, expressas em gramas do sal por 100 gramas de água, em função da temperatura, estão representadas no gráfico a seguir. 2 | Projeto Medicina – www.projetomedicina.com.br Com base nas informações fornecidas, pode-se afirmar corretamente que:
- A) a dissolução dos dois sais em água são processos exotérmicos.
- B) quando se adicionam 50g de KNO3 em 100g de água a 25°C, todo o sólido se dissolve.
- C) a solubilidade do KNO3 é maior que a do NaCl para toda a faixa de temperatura abrangida pelo gráfico.
- D) quando se dissolvem 90g de KNO3 em 100g de água em ebulição, e em seguida se resfria a solução a 20ºC, recupera- se cerca de 30g do sal sólido.
- E) a partir de uma amostra contendo 95g de KNO3 e 5g de NaCl, pode-se obter KNO3 puro por cristalização fracionada.
8) (Unifesp-2002) Para se isolar a cafeína (sólido, em condições ambientais) de uma bebida que a contenha (exemplos: café, chá, refrigerante etc.) pode-se usar o procedimento simplificado seguinte. “Agita-se um certo volume da bebida com dicloroetano e deixa-se em repouso algum tempo. Separa-se, então, a parte orgânica, contendo a cafeína, da aquosa. Em seguida, destila-se o solvente e submete-se o resíduo da destilação a um aquecimento, recebendo-se os seus vapores em uma superfície fria, onde a cafeína deve cristalizar.” Além da destilação e da decantação, quais operações são utilizadas no isolamento da cafeína?
- A) Flotação e ebulição.
- B) Flotação e sublimação.
- C) Extração e ebulição.
- D) Extração e sublimação.
- E) Levigação e condensação.
9) (UNICAMP-2009) As provas de natação da Olimpíada de Beijing foram realizadas no complexo aquático denominado “Water Cube”. O volume de água de 16.000 m 3 desse conjunto passa por um duplo sistema de filtração e recebe um tratamento de desinfecção, o que permite a recuperação quase total da água. Além disso, um sistema de ventilação permite a eliminação de traços de aromas das superfícies aquáticas.
- a) O texto acima relata um processo de separação de misturas. Dê o nome desse processo e explique que tipo de mistura ele permite separar.
- b) A desinfecção da água é realizada por sete máquinas que transformam o gás oxigênio puro em ozônio. Cada máquina é capaz de produzir cerca de 240 g de ozônio por hora. Considerando-se essas informações, qual a massa de gás oxigênio consumida por hora no tratamento da água do complexo?
10) (Unicamp-2005) Pode-se imaginar que o ser humano tenha pintado o próprio corpo com cores e formas, procurando imitar os animais multicoloridos e assim adquirir as suas qualidades: a rapidez da gazela; a força do tigre; a leveza das aves… A pintura corporal é ainda muito usada entre os índios brasileiros. Os desenhos, as cores e as suas combinações estão relacionados com solenidades ou com atividades a serem realizadas. Para obter um corante vermelho, com o que pintam o corpo, os índios brasileiros trituram sementes de urucum, fervendo esse pó com água. A cor preta é obtida da fruta jenipapo ivá. O suco que dela é obtido é quase incolor, mas depois de esfregado no corpo, em contato com o ar, começa a escurecer até ficar preto.
- a) No caso do urucum, como se denomina o processo de obtenção do corante usando água?
- b) Cite dois motivos que justifiquem o uso de água quente em lugar de água fria no processo extrativo do corante vermelho.
- c) Algum dos processos de pintura corporal, citados no texto, envolve uma transformação química? Responda sim ou não e justifique.
11) (UFSE-1997) Considere amostras de: I. petróleo II. água potável III. ar liquefeito IV. latão Destilação fracionada é o processo apropriado para separar os componentes de:
- a) I e II.
- b) I e III.
- c) II e III.
- d) II e IV.
- e) III e IV.
12) (UFRN-1999) Freqüentemente, toma-se conhecimento de notícias sobre acidentes com navios petroleiros. Os vazamentos de petróleo geralmente são identificados por grandes manchas negras que se formam sobre a superfície dos oceanos, causando sérios prejuízos à vida marinha. Essas manchas ocorrem porque o petróleo é basicamente constituído por uma mistura de
- A) hidrocarbonetos insolúveis em água.
- C) sais solúveis em água.
- B) macromoléculas solúveis em água.
- D) minerais insolúveis em água.
13) (UFRN-1997) O Rio Grande do Norte é o maior produtor brasileiro de cloreto de sódio (usado como sal de cozinha), obtido a partir da água do mar, sob condições favoráveis de incidência solar e de ventos. Na obtenção do cloreto de sódio, dois processos destacam se:
- a) centrifugação e decantação.
- b) decantação e dissolução.
- c) dissolução e evaporação.
- d) evaporação e precipitação.
- e) precipitação e sublimação.


