Propriedades da água
Conteúdos e temas: calor específico; densidade; temperatura de ebulição da água com a presença de solutos; solubilidade; outras propriedades.
Competências e habilidades: reconstruir o conceito de solubilidade em um nível mais amplo, como extensão da dissolução; compreender como as propriedades peculiares da água possibilitam a existência de vida no planeta; concluir, a partir da análise de dados experimentais, como a presença de solutos afeta as propriedades características da água; aplicar esses conhecimentos na resolução de problemas ambientais, industriais e relacionados à saúde.
Estratégias de ensino: leitura e análise de tabelas; interpretação de gráficos; demonstrações experimentais.
Sugestão de recursos: materiais para a realização de experimentos; descrição de experimentos; questões.
Avaliação: trabalhos executados no decorrer das atividades; trabalho individual.
Propriedades da Água
A água nossa de cada dia A água nos parece ser simples demais. Nada mais falso! A água é anormal diferente de todas as outras substâncias.
A água tem características especiais que permitem a vida no planeta, entre elas, sua grande capacidade de dissolver substâncias, além de conter nutrientes orgânicos e inorgânicos, é encontrada em maior quantidade na forma líquida, aspectos essenciais aos seres vivos. Se comparada com o ar, ela possui valores maiores de densidade, resistência à passagem da luz e calor específico.
A água é um líquido estranho. Quando olhamos um copo de água gelada, não percebemos os grandes mistérios que este material guarda. Em um mundo altamente tecnológico, ficamos maravilhados com o silício, que possui a propriedade extraordinária de aumentar a sua condutividade ao ser dopado por pequenas quantidades de outro material. Esta propriedade interessante possibilitou a criação dos chips de computador mais de cem anos depois de ter sido observada pela primeira vez.
Por outro lado, a água nos parece ser simples demais. Nada mais falso! Notem: o silício tem somente uma propriedade diferente do que a maioria dos materiais apresenta, por ser um semicondutor, e já é um sucesso; a água tem mais de 70 comportamentos fora de série, e é, portanto, um material com inúmeras aplicações. Ilustremos um destes comportamentos.
A Estrutura da Molécula da Água
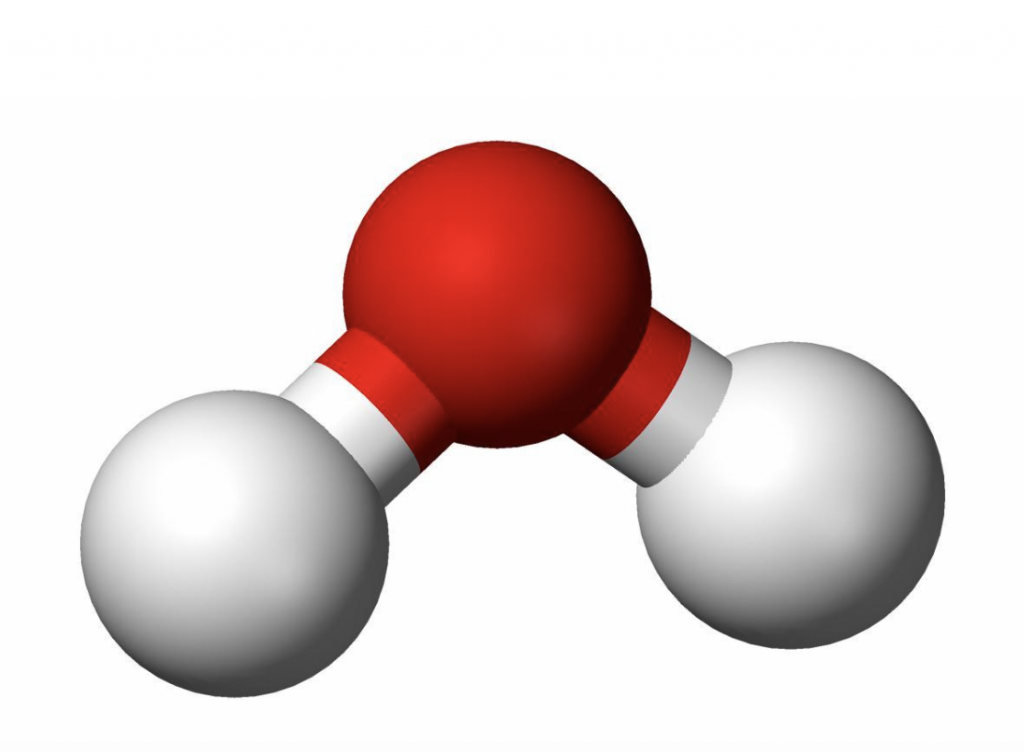
A fórmula da água, H20, indica que é composta por dois átomos de hidrogênio e um de oxigênio. Esses átomos compartilham de forma desigual os elétrons, criando uma polaridade (cargas positivas e negativa). É isso que torna a água tão especial? A molécula de H2O em seu formato simples guarda um segredo.
O oxigênio, com seus oito elétrons, para se equilibrar eletronicamente precisa de mais dois elétrons, enquanto cada hidrogênio, com somente um elétron, precisa de um elétron a mais para se equilibrar. A natureza para resolver esse problema, criou uma negociação perfeita chamada de ligação covalente. O oxigênio empresta um elétron para cada hidrogênio e cada hidrogênio empresta o seu único elétron para o oxigênio.
Em média, cada hidrogênio fica com dois elétrons e cada oxigênio com dez elétrons.
A ligação covalente, no entanto, não é igualitária. O oxigênio por ter mais prótons, puxa todos os elétrons para a sua vizinhança. Os hidrogênios ficam com os elétrons, mas estes não ficam próximos ao H e sim ao O, ficando a molécula polarizada. Surge assim a “ligação de hidrogênio”.
Enquanto a ligação covalente é entre átomos, a de hidrogênio é entre moléculas, sendo esta última bem mais fraca do que a primeira. Se a ligação covalente é um casamento entre o oxigênio e o hidrogênio, a ligação de hidrogênio é um flerte fortuito entre o hidrogênio de uma molécula e o oxigênio da molécula vizinha. Devido ao formato em V das ligações covalentes, como ilustra a figura 1.
cada molécula de água pode formar até quatro ligações de hidrogênio. Imagine você estar no centro de um cubo, com os dois braços apontando para dois vértices em diagonais opostas da face superior do cubo e os dois pés apontando para dois vértices em diagonais opostas na face inferior do cubo, alternadas em relação às superiores, como ilustra a figura 2.
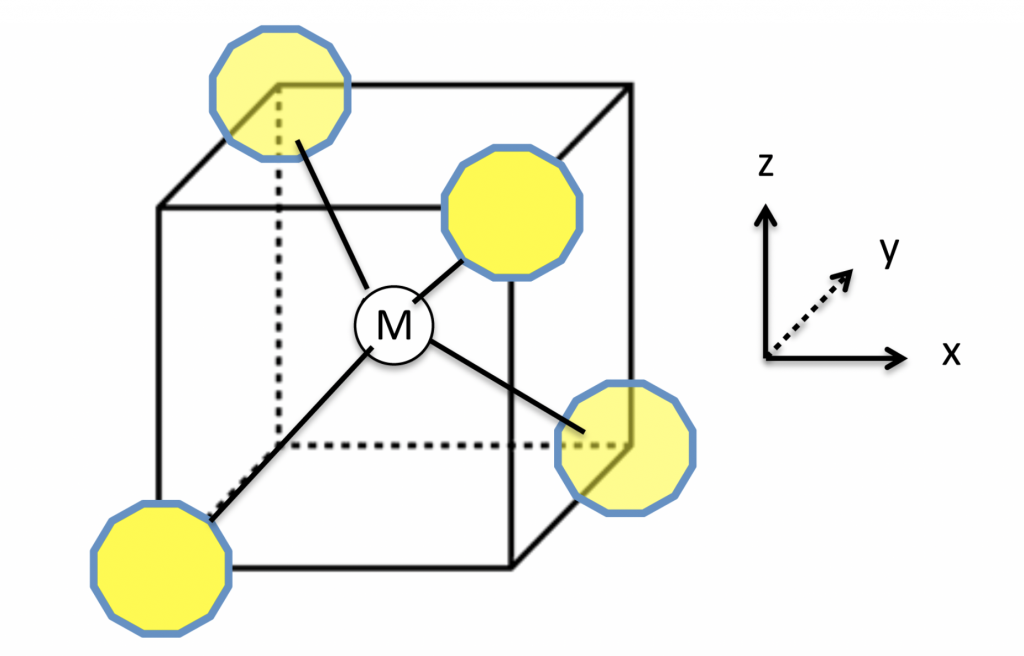
As quatro ligações de hidrogênio são exatamente assim. Note que elas têm uma distância e ângulo bem precisos. Assim, a baixas temperaturas, o gelo forma todas as ligações possíveis, mas ao aumentar a temperatura algumas ligações são rompidas, o que permite que as moléculas se aproximem, aumentando a densidade e, por isso, o gelo é menos denso que a água a 4º C.
A presença das ligações também explica o calor específico elevado, pois é necessário dar calor para romper a ligação e, somente depois de rompida, aumentar a temperatura. Materiais que têm cargas livres, como o sal de cozinha, ou que formam ligações de hidrogênio com a água, como os álcoois, amam a água e se dissolvem bem na água; materiais sem cargas, como os polímeros que usamos para cobrir o sofá da nossa casa, odeiam água e não se solubilizam em água e, por isso, são ótimos para impedir que algo se molhe.Além de propriedades termodinâmicas, a água se move de maneira peculiar.
Em outras palavras, a molécula da água é polar e por isso as moléculas ligam-se através de pontes de hidrogênio, que são bem fortes.
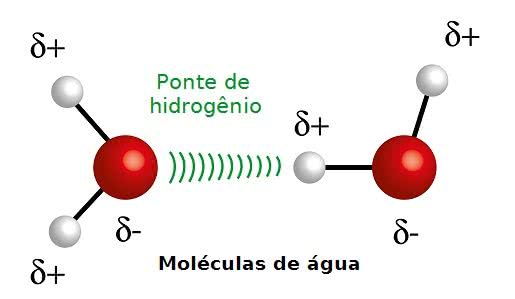
Representação das moléculas de água e a ponte de hidrogênio entre elas. Observe as cargas elétricas.
A água na natureza pode ser encontrada no estado sólido nas geleiras de regiões muito frias, no estado de vapor formando a atmosfera e as nuvens, ou como líquido nos rios, mares e outros corpos aquáticos.
A forma mais abundante na natureza, nas condições normais de temperatura e pressão, é a líquida graças à sua estrutura química, além do fato de ter um alto ponto de ebulição (só ferve aos 100°).
Essas características da molécula da água influenciam várias propriedades químicas e físicas da água, como a tensão superficial, o calor específico, a solubilidade, entre outras, explicadas a seguir.
Densidade
A densidade é uma medida da concentração da massa em certo volume, ou seja, determina o quanto a substância é compacta.
Se você pegar um cubo de gelo e colocar na água líquida, ele flutua, porque gelo é menos denso do que água.
Isto é anormal, pois a fase sólida dos demais materiais é mais densa que sua fase líquida. Uma barra de metal, por exemplo, afunda no metal líquido.
Ainda mais espetacular do que gelo flutuar em água, é água a 0º C flutuar em água a 4º C.
Assim, no inverno, em locais que alcançam temperaturas negativas, os rios e lagos congelam somente na superfície, permitindo que peixes e plantas sobrevivam no fundo, que está a uma temperatura de 4º C.
Isto, inclusive, permitiu que algumas plantas, insetos e pequenos animais tenham sobrevivido a uma das últimas eras glaciais, quando a Terra ficou coberta de gelo.
A densidade da água varia e diminui em temperaturas menores. Isso explica porque o gelo flutua na superfície da água.
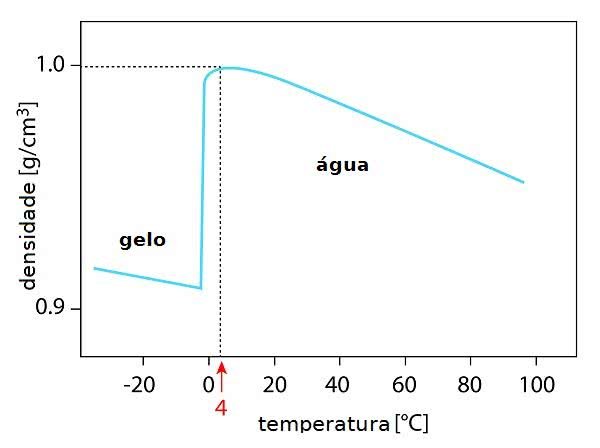
Gráfico mostrando as variações de densidade da água de acordo com a temperatura.
Exemplo: a superfície dos lagos congela devido a essa diferença de densidade em relação ao interior do lago.
Propriedades Físico-Químicas da Água
Solubilidade
A água é um solvente fantástico. Água dissolve bem o sal do nosso sangue e da nossa comida, e o açúcar do nosso café. A água, no entanto, tem seus desafetos. Água detesta compostos apolares (moléculas que, diferentemente da água, são mais democráticas na sua distribuição de elétrons, e não têm acúmulo de cargas em uma dada direção), particularmente óleos.
Para resolver este conflito entre água e óleo, é possível usar moléculas surfactantes, como o detergente de cozinha, que une estes dois grandes inimigos. Este jogo de amor e ódio que certos materiais têm com a água tem sua utilidade. Cobrimos o sofá da sala com um polímero que odeia água para que o mesmo não molhe e usamos materiais que amam água para absorver água do ar como, por exemplo, o sal de cozinha – se o deixamos exposto em um dia úmido, ele transforma o vapor de água em água.
Isto ocorre porque o sal é polar (tem uma distribuição de carga). Em regiões áridas, se usam polímeros com grupos com cargas para fabricar redes que capturam água do ar .
A água é um excelente solvente porque é capaz de dissolver enorme quantidade de substâncias. As substâncias que se dissolvem são chamadas solutos e ao ser misturada com o solvente forma uma solução. Essa propriedade é muito importante para os seres vivos porque absorvem nutrientes (como o cálcio, o magnésio, etc) dissolvidos na água que bebem.
Exemplo: quando o sal é adicionado na água e misturado forma uma solução.
Tensão Superficial
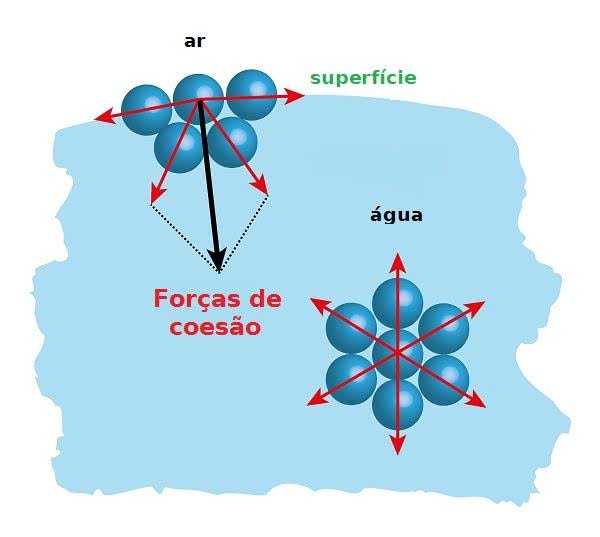
Esquema das forças de coesão nas moléculas da superfície e nas moléculas internas.
A tensão superficial é uma propriedade física que resulta da força de atração entre as moléculas internas e da superfície.
Nas moléculas internas, como as forças são em todas as direções elas se anulam, já na superfície as forças de coesão puxam para os lados e para baixo, desse modo, fazem com que a superfície fique como uma película elástica.

Inseto na “película elástica” formada pela tensão superficial.
Exemplo: um inseto consegue caminhar sobre a água por causa da tensão superficial. Muitos organismos marinhos vivem nessa região da película como os protozoários, as bactérias, os copépodos, entre outros.
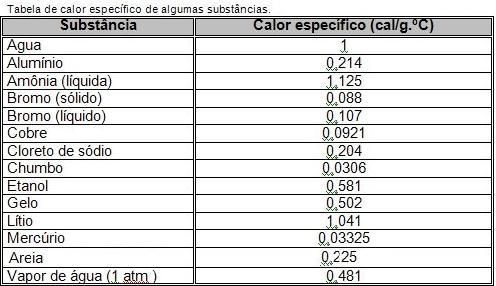
Calor Específico
Outra propriedade fundamental para a vida é o calor específico, Cp, que é quanto calor tem que ser dado para um material aumentar em 1º C a sua temperatura.
No caso da água, o Cp tem um valor alto, o que significa que é necessário dar muito calor para a água aumentar em 1º C a sua temperatura.
Observamos isso quando vamos a uma piscina para nadar. A água durante um dia quente estará mais fria do que o concreto do piso que contorna a piscina, pois, para aumentar a temperatura da água em 1º C, é necessário fornecer mais calor do que para aumentar a temperatura do concreto.
Como a água ocupa cerca de 70% da superfície terrestre, essa propriedade ajuda a controlar o aquecimento do planeta. Os oceanos guardam o calor no tempo quente que é liberado no tempo frio.Esta propriedade extraordinária permite que os oceanos não tenham uma variabilidade de temperatura muito elevada, o que igualmente ajuda na manutenção da vida.
Mas há coisas bem quotidianas nas quais podemos usar esta propriedade. Se queremos esfriar uma panela de pressão bem quente rapidamente, a colocamos em contato com a água, ao invés de a deixarmos em contato com o ar, pois a capacidade de absorver calor da água é maior do que a do ar.
A indústria usa esta anomalia da água – absorver mais calor do que outros materiais – para controle de temperatura.
A água tem um elevado calor específico, o que significa dizer, que ele consegue aumentar ou diminuir bastante sua temperatura sem mudar de estado físico, mas por outro lado isso demora mais a acontecer, se comparado com outras substâncias.
Calor Latente
Representa a quantidade de calor necessária para que a substância mude de estado físico. O calor latente de vaporização e de fusão da água são muito elevados de modo que evita que ela congele ou evapore muito rapidamente.
Exemplo: o elevado calor latente de fusão da água não permite que ela congele rapidamente, evitando assim que os organismos de ambientes frios congelem.
Mobilidade
Na grande maioria dos materiais, a mobilidade das moléculas aumenta com a diminuição da densidade do sistema, pois o espaço para se mover aumenta. Se queremos fazer o óleo fluir mais, aumentamos a temperatura para diminuir a densidade.
Na água, no entanto, a baixas temperaturas a mobilidade aumenta com o aumento da densidade.
As moléculas de água a altas densidades têm ligações de hidrogênio muito promíscuas que se formam e se desfazem rapidamente, permitindo à água se mover de uma molécula vizinha à outra. A água se comporta como um bando de foliões no carnaval, onde a densidade de pessoas é enorme: as pessoas se movem rapidamente, largando o braço de um companheiro de bloco e passando ao braço de outro.
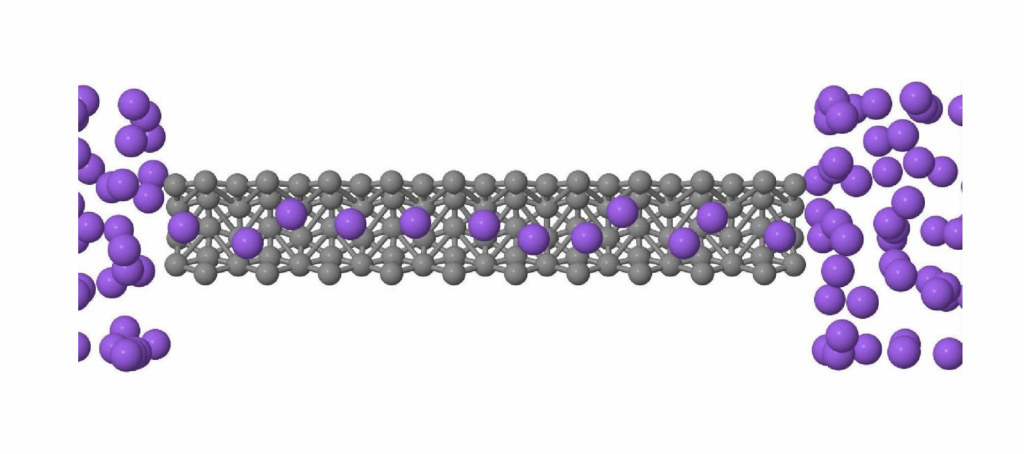
Uma consequência interessante desta alta mobilidade é que se colocarmos a água confinada em tubos muito fininhos (10.000 vezes mais finos do que um fio de cabelo), a água flui através do tubo a uma velocidade que pode ser até 1.000 vezes maior do que se espera para a maioria dos materiais. O que ocorre é que a água confinada em volumes pequenos se move usando a rede de ligações de hidrogênio.
Para um tubo bem fininho, as moléculas formam uma linha compacta, que se move como se fosse um tubo dentro de outro tubo como mostra a figura 3. Este fenômeno tem uma aplicação muito importante.
Qual a utilidade deste superfluxo?
Hoje uma em cada seis pessoas no mundo vive em regiões onde há stress hídrico, ou seja, vivem em regiões que não têm água suficiente para produzir a sua subsistência, e este número em 2030 irá chegar a 50% da população. No Brasil, temos regiões que não têm água suficiente para a sobrevivência, e o crescimento não planejado da agricultura adicionado ao uso indiscriminado de agrotóxicos tem levado a situações de falta de água em regiões como São Paulo.
Este quadro, com o crescimento da população, mudança do clima e contaminação da água potável, irá se agravar mundialmente nos próximos anos.Uma solução que se usa para isso é a dessalinização de água do mar ou salobra. Hoje na Califórnia, em algumas ilhas do Caribe, em diversos países do Oriente Médio e na ilha de Fernando de Noronha, a dessalinização é uma realidade.
Uma alternativa é o processo de osmose reversa, usado na Califórnia, que consiste em empurrar a água através de um filtro que permite a passagem de água, mas não a de sal. Este processo é caro e ineficiente, pois as plantas de dessalinização são instalações enormes e se justificam somente para abastecer grandes cidades, pois o processo não tem um equivalente em pequena escala.
O defeito deste processo é que não usa nenhuma das propriedades mágicas da água.Com a descoberta recente do superfluxo da água confinada, alguns pesquisadores têm proposto o uso de nano estruturas para separar a água do sal. A água atravessa os nanotubos de carbono com um superfluxo e o sal, devido à barreira dielétrica da membrana nanométrica, fica fora da membrana.
Para que o processo ocorra, os poros devem ter 2 nanômetros de diâmetro, o que por si só é um desafio para a produção em série. A boa nova é que testes laboratoriais realizados na Universidade da Califórnia e testes computacionais realizados por diversos grupos, inclusive o do Instituto de Física da Universidade Federal do Rio Grande do Sul que coordeno, mostraram que este processo seria em ordens de grandeza mais eficiente do que aquele usado atualmente, tornando as plantas de dessalinização mais eficientes, exigindo um consumo menor de energia e filtros menores, ou seja, factíveis para pequenas cidades ou mesmo para bairros. Esperamos que com o desenvolvimento de tecnologias de larga escala para a produção de nanotubos, grafeno ou do MoS2 em quantidade suficiente para construir membranas como a ilustrada na figura 4, em dez anos esta tecnologia esteja implementada no mundo ou, quem sabe se voltarmos a ter um financiamento regular e ininterrupto em ciência e tecnologia, mesmo no Brasil.
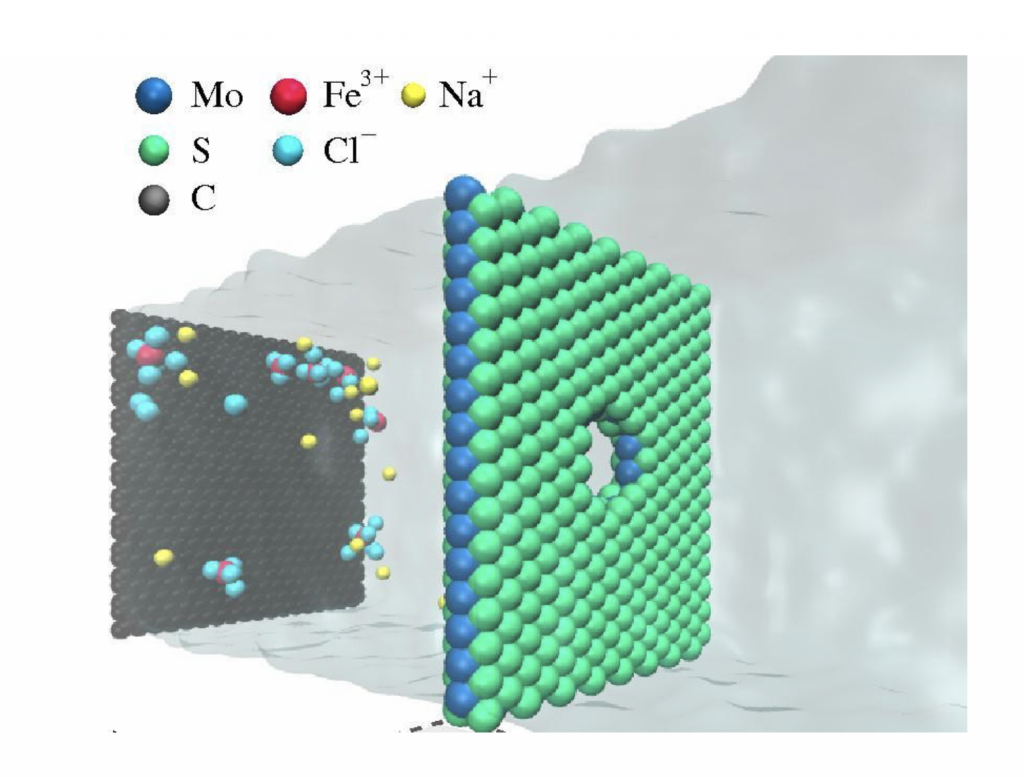
Figura 4 – Sal e água (região sombreada) passando através de uma membrana nanométrica de Dissulfeto de Molibdênio. (Imagem da autora)Dissolução de materiais em água e mudança de suas propriedades
Transporte
Transporte: a água tem a propriedade de transportar líquidos e partículas de substâncias. Essa capacidade de transportar substâncias é vital nos seres vivos, pois o sangue, feito aproximadamente de 60% de água, transporta para diferentes partes do corpo gases (como oxigênio, gás carbônico), hormônios, nutrientes e produtos da excreção.
Propriedades da Água
Água e Vida
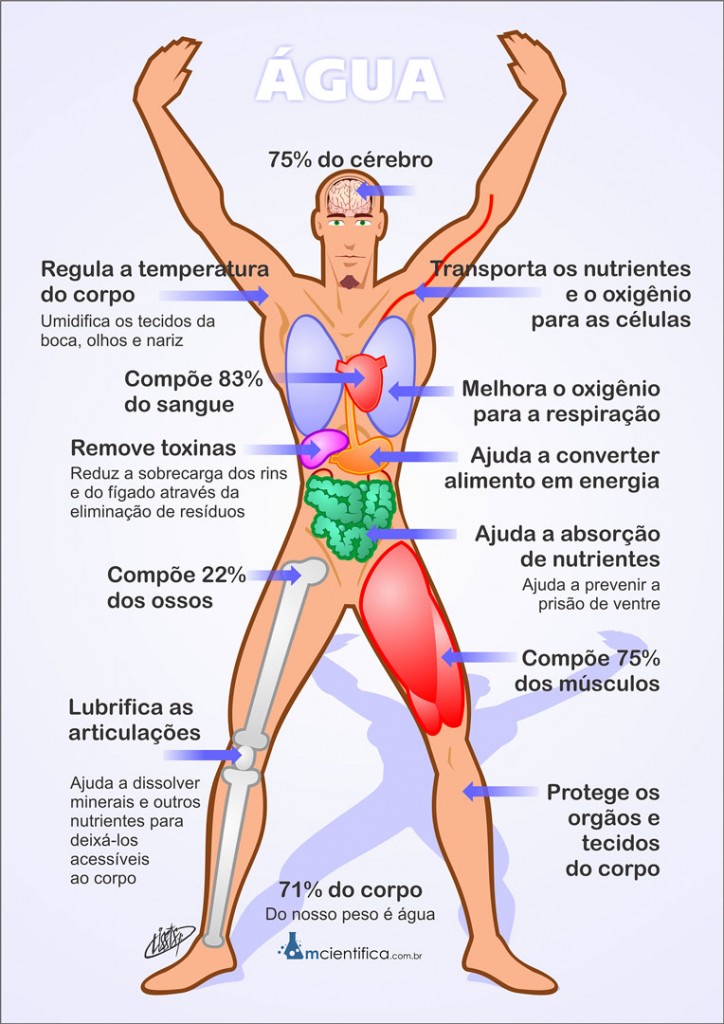
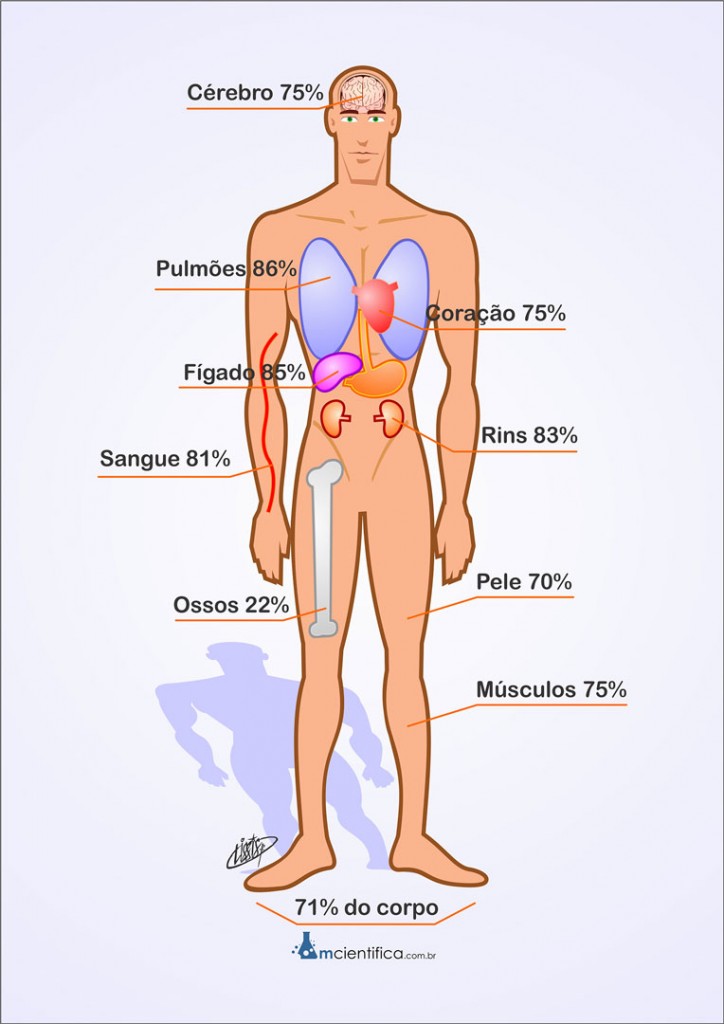
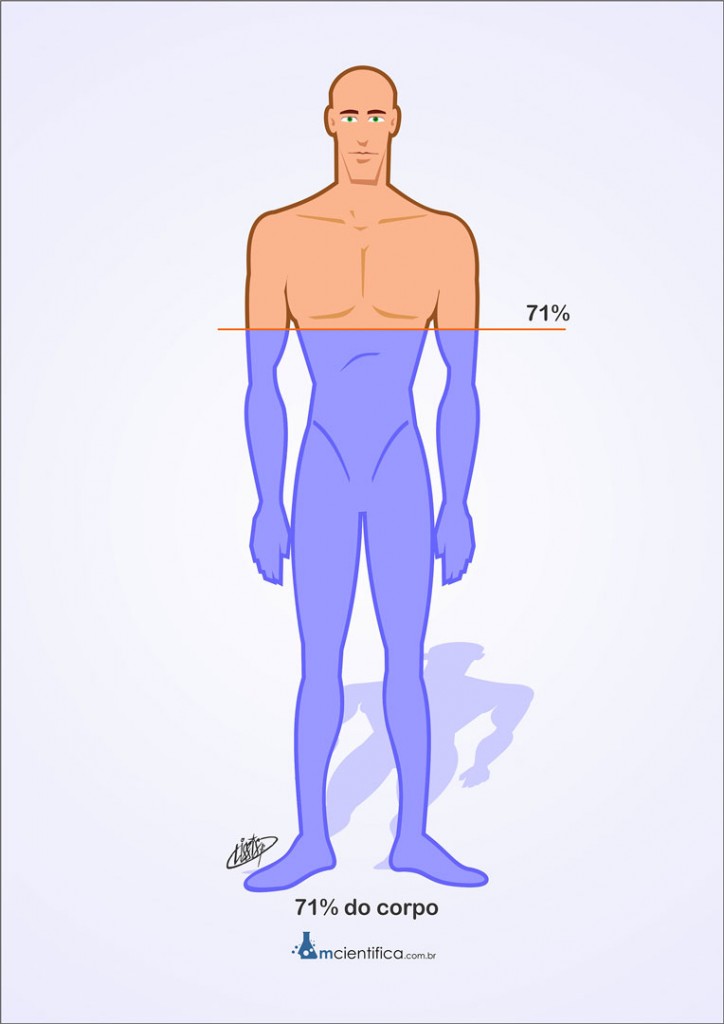
A água é uma substância essencial para a vida dos organismos na Terra. É encontrada em grandes quantidades em todos os seres vivos.
No corpo humano, 71% do nosso peso é água. Contém 85% de água no nosso sangue, 75% no cérebro, 70% na pele e 22% nos nossos ossos.
Nos vegetais, a quantidade de água é maior.
Veja a tabela:
|
ALIMENTOS |
QUANTIDADE EM % DE ÁGUA |
|
COUVE |
90 |
|
CENOURA |
88 |
|
MAÇÃ |
84 |
|
MILHO/FEIJÃO |
15 |
|
TOMATE |
95 |
|
ALFACE |
94 |
|
MORANGO |
89 |
|
BATATA |
77 |
É na água que ocorrem as transformações porque as substâncias estão dissolvidas nela, no nosso corpo. A água é quem transporta e distribui o sangue para o resto do corpo.
Perdemos água através da urina, suor, fezes e expiração.
Toda água eliminada fará falta mais tarde para o nosso organismo, por isso a importância de repor esta água e a importância de sentirmos sede.
Um adulto deve tomar cerca de 2,5 litros de liquido por dia.
PERDA DE LIQUIDO DIARIAMENTE (EM MÉDIA)
|
PERDA DIÁRIA |
QUANTIDADE EM cm³ |
|
URINA |
1250 |
|
SUOR |
650 |
|
EXPIRAÇÃO |
500 |
|
FEZES |
100 |
|
TOTAL |
2500 cm³ = 2,5L |
A água é o composto químico mais abundante na Terra. Pode ser encontrada na natureza em três estados físicos: sólido (gelo), líquido (água líquida) e gasoso (vapor). Algumas das propridades da água estão listadas:
Propriedades da água:
1- A água é inodora (sem cheiro)
2- Ela também é incolor (transparente, cristalizada)
3- A água tem a capacidade de absorver calor servindo de regulador térmico para nosso corpo.
4- O peso da água, 1 Litro equivale a 1000 gramas, ou 1 quilograma.
5- Na forma de gelo, faz uma camada superficial impedindo que o calor saia e mantendo uma temperatura estável. Em sua forma liquida ocupa uma grande área, servindo de base. Em forma de vapor transmite calor para aquecer outros corpos.
6- A água na atmosfera absorve algumas substâncias radiativas do sol, protegendo a vida em nosso planeta.
7- A água dissolve as outras substâncias através de processos de hidrólise. Diminui uma concentração de um soluto em uma quantidade de um determinado volume. Assim podemos eliminar substâncias tóxicas.
8- O vapor d’água é o principal responsável por regular a temperatura de nosso planeta, ao contrário dos gases do efeito estufa como pensamos, assim a grande capacidade da água de absorver calor permite manter as temperaturas altas ao longo das camadas de ar.
9- Realiza trocas químicas dentro de nosso corpo graças a seus íons por isso é essencial sua ingestão pelos seres vivos.
10- Corpos que possuem uma densidade maior que a da água afundam, os demais flutuam, isto é explicado pela força de empuxo, uma espécie de empurrão para cima, que a água exerce nos objetos. Assim um barco pode ficar na superfície, uma pessoa boiar e uma latinha afundar, etc.
Consumo Humano: Água Potável
As propriedades da água destinada ao consumo humano devem seguir os padrões de qualidade para ser uma água potável, esses parâmetros são chamados de potabilidade.
Desse modo, são definidas as quantidades limites de certas substâncias que são prejudiciais à saúde, tais como mercúrio, chumbo, cádmio, bem como agrotóxicos, desinfetantes dentre outros.
Também está determinado o limite de microrganismos, os coliformes fecais, e as características organolépticas, como a turbidez (o quanto a água está turva), a intensidade de odor e gosto.
O Ministério da Saúde publicou a portaria Nº 2914, de dezembro de 2011, que “Dispõe sobre os procedimentos de controle e de vigilância da qualidade da água para consumo humano e seu padrão de potabilidade.”
Essa portaria define a água potável como aquela “destinada à ingestão, preparação e produção de alimentos e à higiene pessoal, independentemente da sua origem“. Esses padrões se aplicam apenas à água proveniente do abastecimento de água e não às águas minerais.