Ligação metálica?O que é ligação metálica? Trata-se da forma como os átomos de um elemento metálico interagem entre si, o que origina diversas propriedades importantes, como a maleabilidade e a ductibilidade.

O metal ouro é constituído a partir de ligações metálicas
Os metais são elementos químicos que apresentam como principal característica física a capacidade de perder elétrons e, consequentemente, formar cátions metálicos. Por essa razão, eles podem realizar dois tipos de ligações químicas: a ligação iônica e a ligação metálica.A ligação iônica ocorre quando um metal interage com um elemento de natureza ametálica, que pode ser um ametal ou o hidrogênio. Nesse tipo de ligação, temos a perda de elétrons por parte dos metais e o ganho de elétrons por parte dos ametais ou do hidrogênio.Já a ligação metálica é estabelecida entre os átomos de um único elemento metálico. Esse tipo de ligação ocorre apenas entre os átomos de um único metal e exclusivamente porque um metal não pode estabelecer ligação química com outro elemento metálico diferente.Características gerais dos metais
- Sólidos em temperatura ambiente, com exceção do mercúrio
- São brilhantes;
- Apresentam elevados pontos de fusão e de ebulição;
- Apresentam, em geral, cor prateada, com exceção do ouro, que é dourado, e do cobre, que é avermelhado;
- Os metais puros são formados por aglomerados de átomos (de um único elemento químico) denominados de retículos cristalinos.
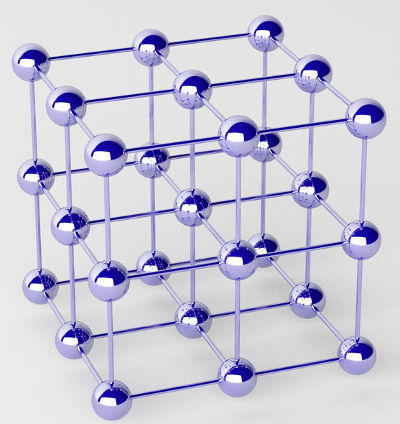
Representação do retículo cristalino de um metalPrincípios da ligação metálicaNa ligação metálica, os retículos cristalinos que formam os metais são, na verdade, um aglomerado iônico (composto apenas por cátions e elétrons). Os elétrons presentes na camada de valência dos átomos do metal são deslocalizados, ou seja, saem da camada de valência, fazendo com que o átomo se torne um cátion (deficiente em elétrons).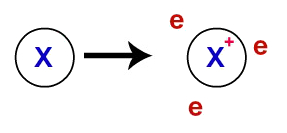
Representação dos elétrons deslocalizados da camada de valênciaApós serem deslocalizados, os elétrons provenientes dos átomos do metal passam a rodear os cátions, formando um verdadeiro “mar de elétrons”. Cada um dos elétrons presentes nesse mar possui capacidade de mover-se por meio do retículo cristalino do metal livremente.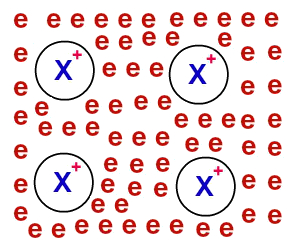
Representação do modelo do mar de elétronsOBS.: Os elétrons “do mar” não são capazes de abandonar o retículo cristalino e movimentam-se por ele.Propriedades dos metais justificadas pela ligação metálicaa) MaleabilidadePor meio de um metal, é possível produzir chapas de diversas espessuras e lâminas. É graças a essa propriedade dos metais que podemos construir diversos objetos, como facas, espadas etc.
A lâmina de uma espada é feita a partir de um metalb) CondutibilidadeOs metais, de uma forma geral, são bons condutores de corrente elétrica e calor. Quando um metal qualquer está em contato com uma fonte de calor ou com uma fonte de corrente elétrica, ele é capaz de conduzi-los.
Uma panela de alumínio na chama de um fogão fica inteiramente quente em virtude da condutividadec) DuctibilidadePor meio de um metal, podemos produzir fios. A utilização de um metal na forma de fios facilita a sua utilização, principalmente em relação à condutibilidade elétrica.
Um metal, como o cobre, pode ser utilizado para a produção de fios
Ligação Metálica

As propriedades de uma ligação são diferentes das propriedades dos seus elementos constituintes. Os metais quando analisados separadamente possuem características únicas que os diferem das demais substâncias: eles são sólidos à temperatura ambiente (25°C) e apresentam cor prateada.
A estrutura atômica dos metais é a Cristalina, que se constitui por cátions do metal envolvidos por uma nuvem de elétrons.
A capacidade que os metais têm de conduzir eletricidade se explica pela presença dessa nuvem de elétrons, que conduz corrente elétrica nos fios de eletricidade, não só neles, mas em qualquer objeto metálico.
As ligas metálicas possuem algumas particularidades que os metais puros não apresentam. Justamente por isso, são produzidas e utilizadas em abundância.
Vejamos as propriedades das ligações metálicas Aumento da dureza: se pegarmos, por exemplo, o elemento Ouro (Au) da forma como é encontrado na natureza não conseguiríamos fabricar nenhum objeto consistente, pois ele é mais maleável que a grande maioria dos metais.
Mas se adicionarmos a ele a prata (Ag) e o cobre (Cu) formaremos uma ligação metálica, aumentando a dureza e permitindo sua utilização para fabricar joias, como anéis, pulseiras, relógios, etc.
Essa liga metálica é também conhecida por Ouro 18 quilates e apresenta 75% em massa de ouro e os outros 25% correspondem à prata e ao cobre.Aumento da resistência mecânica: para fabricar materiais que tenham maior resistência ao manuseio, é preciso recorrer à ligação entre os metais.
O aço, por exemplo, é formado por ferro (Fe) e carbono (C).
Essa liga fica tão resistente que é usada na fabricação de peças metálicas que sofrem tração elevada.
Exemplos:Aço cirúrgico: é usado para a obtenção de instrumentos cirúrgicos, por apresentar alta resistência à oxidação.Aço inox: é uma liga dos metais ferro (Fe), carbono (C), cromo (Cr) e níquel (Ni); é usada para fabricar talheres para cozinha, peças de carro, etc.


