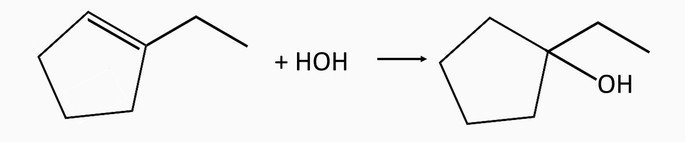Reações Orgânicas
Reações orgânicas são as reações que acontecem entre compostos orgânicos. Há vários tipos de reações. Os principais são: de adição, de substituição, de oxidação e de eliminação.
Elas ocorrem mediante a quebra de moléculas dando origem a novas ligações. Muito utilizadas na indústria, é a partir delas que podem ser produzidos medicamentos e produtos de cosmética, plásticos, dentre tantas outras coisas.
Reação de Adição
A reação de adição acontece quando as ligações da molécula orgânica se rompem e à ela é adicionado um reagente.
Acontece principalmente em compostos cujas cadeias sejam abertas e que tenham insaturações, como alcenos () e alcinos (
).
Confira a seguir exemplos de reações de adição.
Hidrogenação (adição de hidrogênio)
Hidrogenação de um alceno produz um alcano.
Halogenação (adição de halogênios)
Halogenação de um alceno produz um haleto.
Hidratação (adição de água)
Hidratação de um alceno produz um álcool.
Reação de Substituição
A reação de substituição acontece quando há átomos (ou um grupo) ligantes que são substituídos por outros.
Acontece principalmente entre alcanos, ciclanos e aromáticos.
Confira a seguir exemplos de reações de substituição.
Halogenação (substituição por halogênio)
Halogenação de um alcano produz um haleto.
Nitração (substituição por nitro)
Nitração de um alcano produz um nitrocomposto.
Sulfonação (substituição por sulfônicos)
Sulfonação de um alcano produz um ácido.
Reação de Oxidação
A reação de oxidação, também chamada de oxirredução, acontece quando há ganho ou perda de elétrons.
Confira a seguir exemplos de reações de oxidação.
Oxidação enérgica dos alcenos
Oxidação enérgica de um alceno produz ácidos carboxílicos.
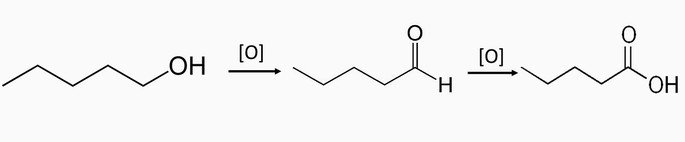
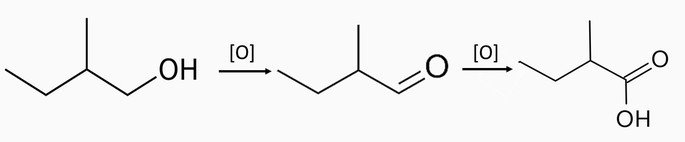
Oxidação de álcool primário
Oxidação enérgica de um álcool primário produz ácido carboxílico e água.
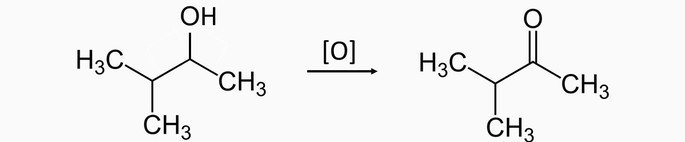
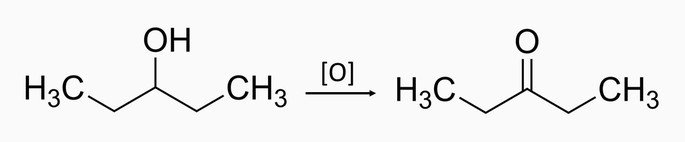
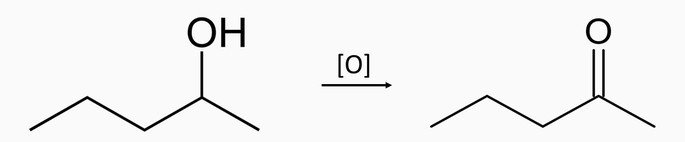
Oxidação de álcool secundário
Oxidação de um álcool secundário produz cetona e água.
Reação de Eliminação
A reação de eliminação acontece quando um ligante de carbono é eliminado da molécula orgânica.
Essa reação é contrária à reação de adição.
Confira a seguir exemplos de reações de eliminação.
Eliminação de hidrogênio (desidrogenação)
Eliminação de hidrogênio de um alcano produz um alceno.
Eliminação de halogênios (de-halogenação)
Eliminação de halogênios de um di-haleto produz um alceno.
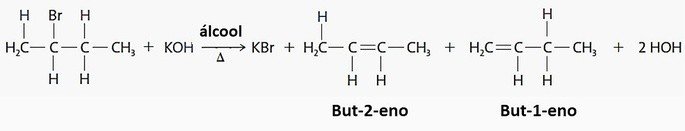
Eliminação de halogenidreto
Eliminação de halogenidreto de um haleto produz um alceno.
Eliminação de água (desidratação de álcool)
Eliminação de água de um álcool produz um alceno.
Esterificação
A esterificação é uma reação química reversível entre um ácido carboxílico e um álcool, produzindo éster e água.
A reação pode ser descrita da seguinte forma:
ÁCIDO CARBOXÍLICO + ÁLCOOL → ÉSTER + ÁGUA
A reação de esterificação é lenta, sendo necessário um aumento de temperatura e a presença de um catalisador para acelerar a sua velocidade. Esse processo é denominado de Esterificação de Fischer.
A reação inversa a de esterificação é denominada de Hidrólise de Ester. No caso, a partir de éster e água são produzidos ácido carboxílico e álcool.
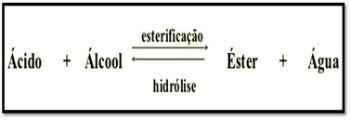
Reações de esterificação
A equação geral de uma reação de esterificação é da seguinte forma:
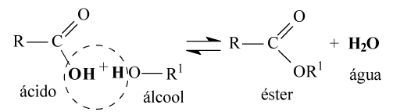
Note que a água é formada pela união do grupo hidroxila (OH) do ácido carboxílico com o hidrogênio (H) do álcool.
O restante da cadeia carbônica do ácido carboxílico e do álcool se unem para originar o éster.
A esterificação também pode ocorrer entre um ácido inorgânico ou álcool secundário ou terciário.
Nesse caso, a formação da água ocorrerá de forma diferente: o grupo hidroxila será proveniente do álcool e o hidrogênio do ácido.
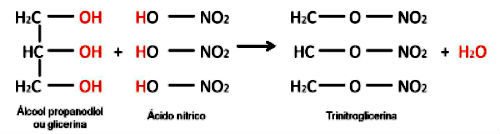
Um exemplo é a reação entre um ácido inorgânico e a formação de um éster inorgânico. As três moléculas de ácido orgânico (ácido nítrico) reagem com a glicerina e forma-se a trinitroglicerina (éster nitrato), um explosivo.
Aplicações
A obtenção de ésteres é importante para produção de diversos tipos de produtos. Veja alguns exemplos:
Aromatizantes em indústrias alimentícias
A esterificação de Fischer é o principal meio para produção de ésteres nas industriais, especialmente alimentícias.
Os flavorizantes são ésteres que conferem aroma e sabor aos produtos industrializados como balas, doces, refrigerantes e sucos.
São exemplos de éster usados como aromatizantes:
- Etanoato de etila: aroma de maçã
- Etanoato de octila: aroma de laranja
- Butanoato de etila: aroma de abacaxi
Biodiesel
O biodiesel é obtido através de uma reação de transesterificação.
O processo consiste na mistura de óleo vegetal ou gordura animal (triglicerídeos) em metanol ou etanol, na presença de um catalisador.
Um dos produtos da reação é a glicerina que pode ser aproveitada para fabricação de cosméticos, alimentos e medicamentos.
Exercícios sobre reações orgânicas
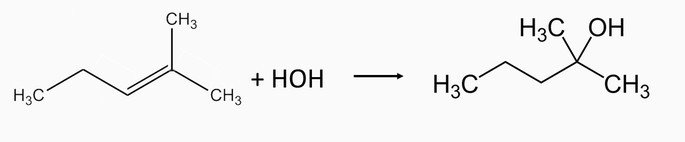
1. (Unifesp/2002) Muitos álcoois podem ser obtidos pela hidratação catalisada por ácidos, de alcenos.
Nessa reação de adição, o H da água se adiciona ao carbono que tem mais hidrogênios ligados a ele e o grupo hidroxila se liga ao carbono menos hidrogenado (regra de Markovnikov).
Sabendo-se que os álcoois formados na hidratação de dois alcenos são respectivamente 2-metil-2-pentanol e 1-etilciclopentanol, quais os nomes dos alcenos correspondentes que lhes deram origem?
a) 2-metil-2-penteno e 2-etilciclopenteno.
b) 2-metil-2-penteno e 1-etilciclopenteno.
c) 2-metil-3-penteno e 1-etilciclopenteno.
d) 2-metil-1-penteno e 2-etilciclopenteno.
e) 3-metil-2-penteno e 2-etilciclopenteno.
2. (Ufal/2000) No estudo da química dos compostos de carbono, aprende-se que o BENZENO:
( ) É hidrocarboneto.
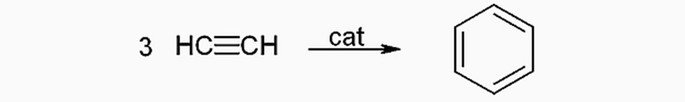
( ) Pode ser obtido a partir do acetileno.
( ) No petróleo, é componente de maior proporção em massa.
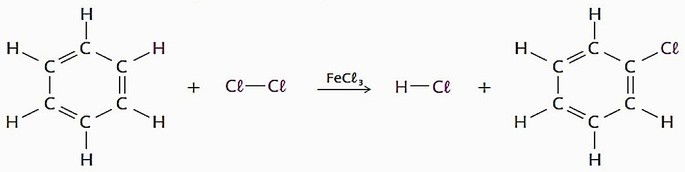
( ) Pode sofrer reação de substituição.
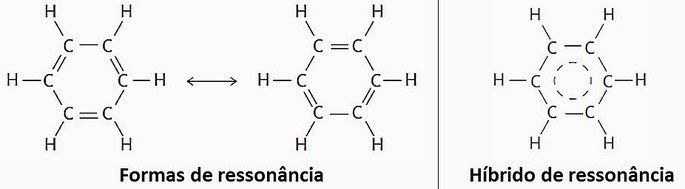
( ) É exemplo de uma estrutura molecular que apresenta ressonância.
Assinale a opção que apresenta a correlação CORRETA entre o nome do álcool e o nome do produto formado.
a) 3-metilbutan-2-ol, 3-metilbutanal
b) pentan-3-ol, pentan-3-ona
c) pentan-1-ol, pentan-1-ona
d) pentan-2-ol, pentanal
e) 2-metilbutan-1-ol, 2-metilbutan-1-ona
Um deles, que se forma em menor quantidade, é o 1-buteno. O outro é o:
a) metilpropeno.
b) 1-butanol.
c) butano.
d) ciclobutano.
e) 2-buteno.
Reações Orgânicas
Reações orgânicas são as reações que acontecem entre compostos orgânicos. Há vários tipos de reações. Os principais são: de adição, de substituição, de oxidação e de eliminação.
Elas ocorrem mediante a quebra de moléculas dando origem a novas ligações. Muito utilizadas na indústria, é a partir delas que podem ser produzidos medicamentos e produtos de cosmética, plásticos, dentre tantas outras coisas.
Reação de Adição
A reação de adição acontece quando as ligações da molécula orgânica se rompem e à ela é adicionado um reagente.
Acontece principalmente em compostos cujas cadeias sejam abertas e que tenham insaturações, como alcenos () e alcinos (
).
Confira a seguir exemplos de reações de adição.
Hidrogenação (adição de hidrogênio)
Hidrogenação de um alceno produz um alcano.
Halogenação (adição de halogênios)
Halogenação de um alceno produz um haleto.
Hidratação (adição de água)
Hidratação de um alceno produz um álcool.
Reação de Substituição
A reação de substituição acontece quando há átomos (ou um grupo) ligantes que são substituídos por outros.
Acontece principalmente entre alcanos, ciclanos e aromáticos.
Confira a seguir exemplos de reações de substituição.
Halogenação (substituição por halogênio)
Halogenação de um alcano produz um haleto.
Nitração (substituição por nitro)
Nitração de um alcano produz um nitrocomposto.
Sulfonação (substituição por sulfônicos)
Sulfonação de um alcano produz um ácido.
Reação de Oxidação
A reação de oxidação, também chamada de oxirredução, acontece quando há ganho ou perda de elétrons.
Confira a seguir exemplos de reações de oxidação.
Oxidação enérgica dos alcenos
Oxidação enérgica de um alceno produz ácidos carboxílicos.
Oxidação de álcool primário
Oxidação enérgica de um álcool primário produz ácido carboxílico e água.
Oxidação de álcool secundário
Oxidação de um álcool secundário produz cetona e água.
Reação de Eliminação
A reação de eliminação acontece quando um ligante de carbono é eliminado da molécula orgânica.
Essa reação é contrária à reação de adição.
Confira a seguir exemplos de reações de eliminação.
Eliminação de hidrogênio (desidrogenação)
Eliminação de hidrogênio de um alcano produz um alceno.
Eliminação de halogênios (de-halogenação)
Eliminação de halogênios de um di-haleto produz um alceno.
Eliminação de halogenidreto
Eliminação de halogenidreto de um haleto produz um alceno.
Eliminação de água (desidratação de álcool)
Eliminação de água de um álcool produz um alceno.
Esterificação
A esterificação é uma reação química reversível entre um ácido carboxílico e um álcool, produzindo éster e água.
A reação pode ser descrita da seguinte forma:
ÁCIDO CARBOXÍLICO + ÁLCOOL → ÉSTER + ÁGUA
A reação de esterificação é lenta, sendo necessário um aumento de temperatura e a presença de um catalisador para acelerar a sua velocidade. Esse processo é denominado de Esterificação de Fischer.
A reação inversa a de esterificação é denominada de Hidrólise de Ester. No caso, a partir de éster e água são produzidos ácido carboxílico e álcool.

Reações de esterificação
A equação geral de uma reação de esterificação é da seguinte forma:

Note que a água é formada pela união do grupo hidroxila (OH) do ácido carboxílico com o hidrogênio (H) do álcool.
O restante da cadeia carbônica do ácido carboxílico e do álcool se unem para originar o éster.
A esterificação também pode ocorrer entre um ácido inorgânico ou álcool secundário ou terciário.
Nesse caso, a formação da água ocorrerá de forma diferente: o grupo hidroxila será proveniente do álcool e o hidrogênio do ácido.
Um exemplo é a reação entre um ácido inorgânico e a formação de um éster inorgânico. As três moléculas de ácido orgânico (ácido nítrico) reagem com a glicerina e forma-se a trinitroglicerina (éster nitrato), um explosivo.

Aplicações
A obtenção de ésteres é importante para produção de diversos tipos de produtos. Veja alguns exemplos:
Aromatizantes em indústrias alimentícias
A esterificação de Fischer é o principal meio para produção de ésteres nas industriais, especialmente alimentícias.
Os flavorizantes são ésteres que conferem aroma e sabor aos produtos industrializados como balas, doces, refrigerantes e sucos.
São exemplos de éster usados como aromatizantes:
- Etanoato de etila: aroma de maçã
- Etanoato de octila: aroma de laranja
- Butanoato de etila: aroma de abacaxi
Biodiesel
O biodiesel é obtido através de uma reação de transesterificação.
O processo consiste na mistura de óleo vegetal ou gordura animal (triglicerídeos) em metanol ou etanol, na presença de um catalisador.
Um dos produtos da reação é a glicerina que pode ser aproveitada para fabricação de cosméticos, alimentos e medicamentos.
São simbolizados por [O] e podem ser o permanganato de potássio (KMnO4), dicromato de potássio (K2Cr2O7) ou o tetraóxido de ósmio (OsO4).
As reações mais importantes de oxidação são as seguintes:
– oxidação energética dos alcenos
– oxidação de álcool primário
– oxidação de álcool secundário
Oxidação energética dos alcenos
Esta oxidação ocorre nos alcenos em contato com um agente oxidante em solução aquosa, concentrada e ácida (geralmente em ácido sulfúrico).
Nesta reação, podemos obter vários produtos, dependendo do tipo da posição da ligação dupla. Observe:
– carbono primário produz gás carbônico e água
– carbono secundário produz ácido carboxílico
– carbono terciário produz cetona
Esta reação serve como teste de insaturação de alceno, ou seja, para identificar que tipo de alceno se tem. Acompanhe o exemplo:

Veja outro exemplo envolvendo carbonos terciários:

Oxidação de álcoois primários
Os álcoois primários se oxidam com oxidantes energéticos, como o permanganato de potássio e dicromato de potássio, em meio sulfúrico.
O produto desta oxidação é aldeído. Com mais quantidade de agente oxidante, obtemos um ácido carboxílico.
Esta reação explica porque o vinho fica com gosto de vinagre quando o deixamos muito tempo em contato com o ar (oxigênio). O álcool sofre uma oxidação e tranforma-se em vinagre, que é um ácido carboxílico.
Exemplo:

Oxidação de álcoois secundários
Os álcoois secundários têm como produto as cetonas. Exemplo:

Observação: Não existe oxidação de álcool terciário.
Exercícios sobre reações orgânicas
1. (Unifesp/2002) Muitos álcoois podem ser obtidos pela hidratação catalisada por ácidos, de alcenos.
Nessa reação de adição, o H da água se adiciona ao carbono que tem mais hidrogênios ligados a ele e o grupo hidroxila se liga ao carbono menos hidrogenado (regra de Markovnikov).
Sabendo-se que os álcoois formados na hidratação de dois alcenos são respectivamente 2-metil-2-pentanol e 1-etilciclopentanol, quais os nomes dos alcenos correspondentes que lhes deram origem?
a) 2-metil-2-penteno e 2-etilciclopenteno.
b) 2-metil-2-penteno e 1-etilciclopenteno.
c) 2-metil-3-penteno e 1-etilciclopenteno.
d) 2-metil-1-penteno e 2-etilciclopenteno.
e) 3-metil-2-penteno e 2-etilciclopenteno.
2. (Ufal/2000) No estudo da química dos compostos de carbono, aprende-se que o BENZENO:
( ) É hidrocarboneto.
( ) Pode ser obtido a partir do acetileno.
( ) No petróleo, é componente de maior proporção em massa.
( ) Pode sofrer reação de substituição.
( ) É exemplo de uma estrutura molecular que apresenta ressonância.
Assinale a opção que apresenta a correlação CORRETA entre o nome do álcool e o nome do produto formado.
a) 3-metilbutan-2-ol, 3-metilbutanal
b) pentan-3-ol, pentan-3-ona
c) pentan-1-ol, pentan-1-ona
d) pentan-2-ol, pentanal
e) 2-metilbutan-1-ol, 2-metilbutan-1-ona
Um deles, que se forma em menor quantidade, é o 1-buteno. O outro é o:
a) metilpropeno.
b) 1-butanol.
c) butano.
d) ciclobutano.
e) 2-buteno.