A BIOSFERA COMO FONTE DE ALIMENTOS PARA O SER HUMANO
Conteúdos e temas: componentes nutricionais dos alimentos; propriedades e funções orgânicas encontradas em carboidratos, lipídios e proteínas; nutrição e saúde. Competências e habilidades: reconhecer as funções orgânicas presentes nos diferentes grupos de alimentos; reconhecer polímeros, assim como os monômeros que os compõem. Sugestão de estratégias de ensino: retomada da análise de rótulos de alimentos realizada em Biologia, focalizando os valores energéticos de cada componente e sua relação com as respectivas estruturas; discussões relacionadas às funções de cada grupo de alimentos na manutenção da vida. Sugestão de recursos: questões; observação de estruturas; livro didático. Sugestão de avaliação: participação em aula; realização das atividades; respostas aos exercícios.
Estudo do Carbono
Química Orgânica
 A Química Orgânica ajuda-nos a entender as estruturas e as propriedades das moléculas formadas por cadeias carbônicas
A Química Orgânica ajuda-nos a entender as estruturas e as propriedades das moléculas formadas por cadeias carbônicasA Química Orgânica recebeu inicialmente esse nome para descrever substâncias extraídas de organismos vivos. Acreditava-se que elas só podiam ser produzidas em organismos vegetais e animais, mas nunca em laboratório. Entretanto, provou-se que o homem conseguia sim sintetizar compostos orgânicos em laboratório, e então a definição de Química Orgânica mudou para:
“Ramo da Química que estuda a maioria dos compostos formados pelo elemento carbono”.
Visto que o carbono é tetravalente, podendo realizar quatro ligações de diferentes maneiras, com átomos de outros elementos ou com átomos do próprio carbono, existem milhões de seus compostos. Uma quantidade muito superior do que a de compostos inorgânicos conhecidos atualmente.
Tais compostos são agrupados em diferentes funções que apresentam propriedades químicas semelhantes, tais como os hidrocarbonetos, os álcoois, as cetonas, os aldeídos, os ácidos carboxílicos, os ésteres, os éteres, as aminas, as amidas, entre outros, como ocorre o fenômeno da isomeria em muitas dessas substâncias e o que são os polímeros naturais e artificiais que formam os plásticos tão comuns em nosso cotidiano.
Composição: o Cé o principal elemento, incluem também o H, N, O, S, P e ainda os halogênios.
Características: em geral os compostos orgânicos são covalentes apolares. A presença de um elemento diferente do C e H promove certa polaridade na molécula.
H H
Ex.: H – C – H H – C – OH
H H
Apolar Polar
CARACTERÍSTICAS GERAIS
Ponto de fusão e ebulição: inferiores aos compostos inorgânicos, a maioria apresenta instabilidade térmica.
Isomeria: compostos com a mesma fórmula molecular.
Solubilidade: os apolares pouco solúveis em água, os polares solúveis, a exemplo do álcool e açúcar.
Combustibilidade: em geral são combustíveis.
Encadeamento: em função da tetravalência do C tendem a formar estruturas denominadas cadeias carbônicas.
Velocidade de reação: pouco reativos, dependem de ativadores (luz, calor, pressão, catalisadores, etc.).
Postulados de Couper – Kekulé
Tais postulados foram propostos no século XIX e são resultantes do trabalho de diversos cientistas, em especial, do químico Archibald Scott Couper e, claro, do próprio Kekulé. Assim, é comum também denomina-los Postulados de Couper-Kekulé.
Postulados do Carbono
Por que é importante estudar a fundo o Carbono? Este elemento é a unidade fundamental dos compostos orgânicos, tudo se explica por suas propriedades únicas.
O comportamento químico do carbono começou a ser explicado através dos estudos de dois cientistas do século XIX, Archibald Scott Couper (1831-1892) e Friedrich August Kekulé (1829-1896). Estes estudiosos deram nome aos postulados de “Couper-Kekulé”, vamos conhecer agora as propriedades do carbono detalhadas por este conceito:
1° postulado: O átomo de carbono é tetravalente
A tetravalência do carbono é sua propriedade de formar quatro ligações covalentes, ou seja, ele disponibiliza quatro elétrons ligantes. Isso porque em sua camada de valência o átomo de carbono possui 4 elétrons livres.
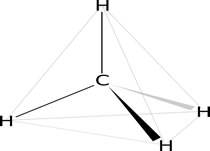
Metano: molécula formada pela ligação de 4 átomos de Hidrogênio (H) a 1 átomo de carbono (C).
2° postulado: As quatro unidades de valência do carbono são iguais entre si.
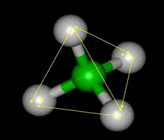
O Fluorometano é um exemplo desta propriedade, só existe um composto com este nome, ele é formado pela substituição de um hidrogênio da molécula de Metano por um átomo de Flúor (F). O Flúor poderá substituir qualquer H da molécula que receberá a mesma nomenclatura, repare na ilustração abaixo:
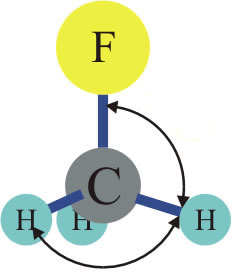
Qualquer posição ocupada pelo átomo de Flúor dará origem ao Fluorometano.
3° postulado: Propriedade de encadeamento – capacidade que átomos de um mesmo elemento têm de formar cadeias moleculares.
.jpg)
Átomos de carbono ligam-se diretamente entre si, formando estruturas denominadas cadeias carbônicas. A variedade de compostos orgânicos existentes na natureza se deve a esta propriedade do Carbono de formar cadeias. O composto acima (decano) é formado por 10 átomos de C interligados.
O carbono não é o único elemento químico que pode formar encadeamentos: alguns outros elementos como o enxofre e o nitrogênio, por exemplo, também apresentam essa característica. No entanto, somente o carbono pode constituir cadeias tão diversificadas, extensas e quimicamente estáveis.
A tetravalência do carbono, sua capacidade de se ligar com vários tipos de elementos químicos e de formar cadeias carbônicas são as propriedades responsáveis pelo enorme número de compostos orgânicos já conhecidos. Por isso, a Química Orgânica é definida como a área da Química que trata dos compostos de carbono com características específicas.
Classificação do Carbono
A classificação do carbono é baseada na quantidade dos demais átomos de carbono ligado a ele e também no tipo de ligação.
O carbono pode ser classificado seguindo vários critérios: um deles se baseia na quantidade dos demais átomos de carbono a ele ligados.
Carbono primário: ligado diretamente, no máximo, a 1 outro carbono;
Carbono secundário: ligado diretamente a 2 outros carbonos
Carbono terciário: ligado diretamente a 3 outros carbonos;
Carbono quaternário: ligado diretamente a 4 outros carbonos.
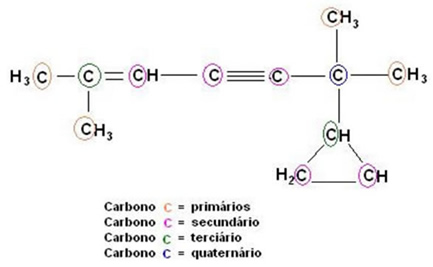
A outra classificação se refere aos tipos de ligação que unem os carbonos.
O carbono pode ser classificado em função das ligações que apresenta:
a) Carbono Saturado: apresenta somente ligações simples, chamadas de sigma (σ).
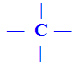
b) Carbono Insaturado: presença de duplas ligações, denominadas de pi (π). Ou ainda, carbono que apresenta ligação tripla.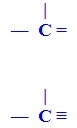
Classificação da Cadeia carbônica
Para representar as cadeias carbônicas de maneira mais simples, é comum utilizar a notação em bastão, que indica cada ligação entre carbonos por traços (—) e cada carbono se transforma em um ponto de inflexão ou nas extremidades dos traços.
Cadeia carbônica é o conjunto de todos os átomos de carbono e de todos os heteroátomos que constituem a molécula de qualquer composto orgânico.
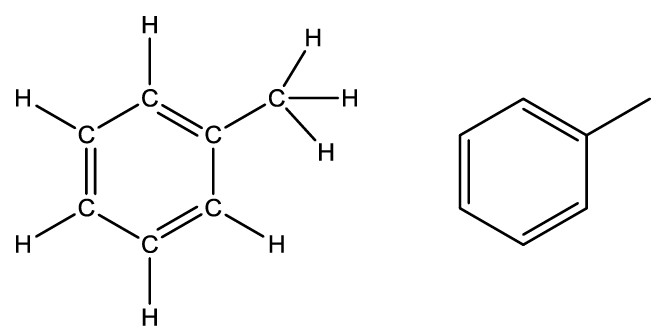
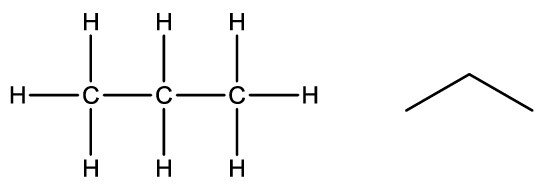
Outra maneira de simplificar a representação, podemos indicar, por meio de índices, a quantidade de átomos de hidrogênio e carbono presente na estrutura:
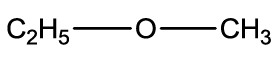
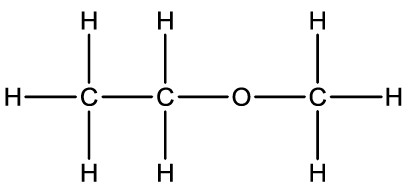
Classificação dos carbonos na cadeia
– Carbono secundário: todos os carbonos que se ligam a dois outros carbonos;
– Carbono terciário: todos os carbonos que se ligam a três outros carbonos;
– Carbono quaternário: carbonos que se ligam a quatro outros carbonos;Carbonos saturados
São os carbonos que apenas realizam ligações covalentes simples com outros carbonos. Sendo assim, todos os carbonos quaternários, são saturados.Carbonos insaturados
São aqueles que fazem ou uma ligação dupla, ou duas duplas ou uma tripla.
Carbono assimétrico
É chamado de carbono assimétrico o carbono que fizer ligações com quatro ligantes diferentes. Ligantes são considerados toda a parte da cadeia que se extende de uma ligação. Na figura abaixo, o carbono destacado é assimétrico, e circulados estão os seus quatro ligantes:
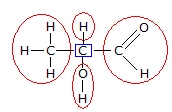
A figura abaixo ilustra as classificações citadas acima:
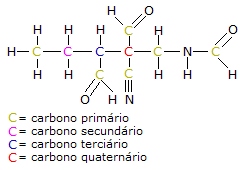
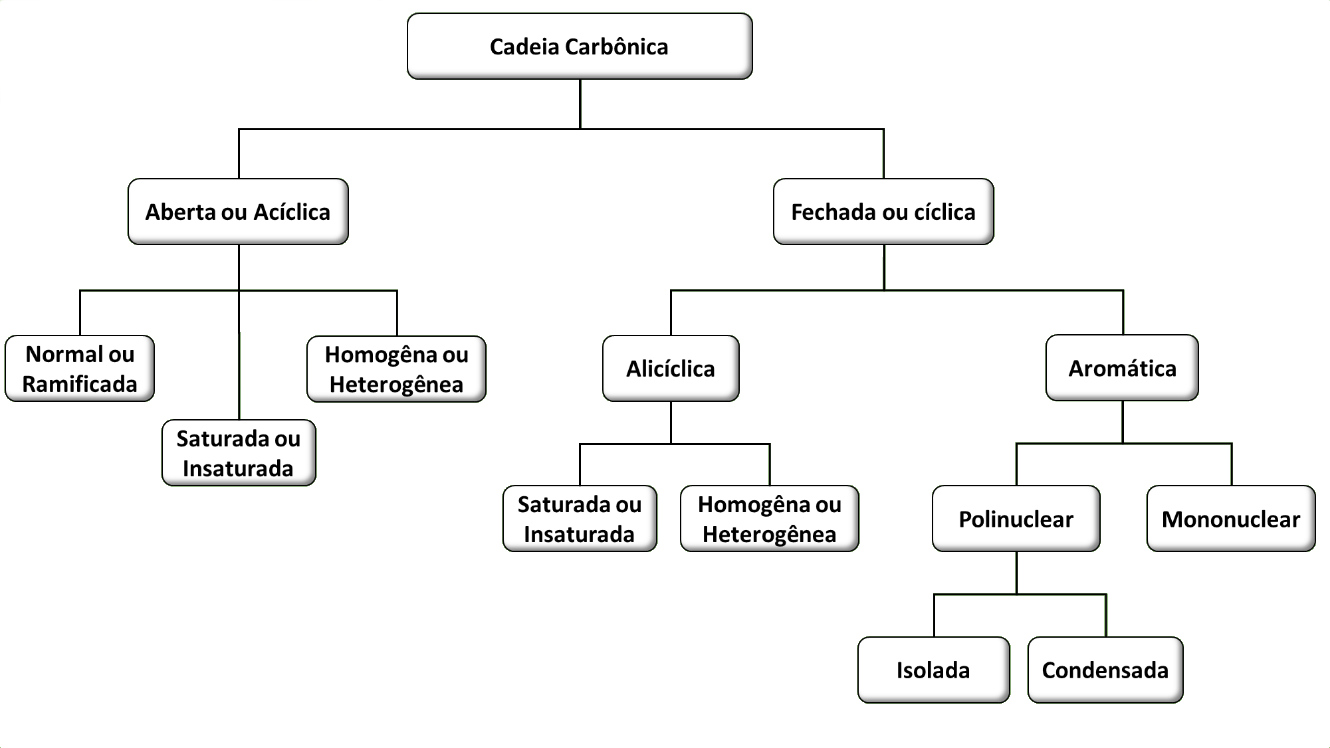
Classificação das cadeias carbônicas
As cadeias carbônicas podem se classificam através de vários fatores:
1- Cadeia aberta ou acíclica
Nessa cadeia, os átomos de carbono não formam ciclo.
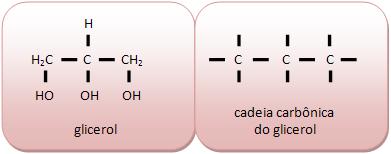
Cadeia fechada ou cíclica
Nessa cadeia, os átomos de carbono formam ciclo ou anéis.
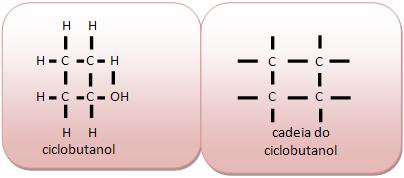
II) Classificação das cadeias acíclicas ou abertas
A) Quanto à disposição dos átomos
Cadeia acíclica normal ou reta:
A única que apresenta átomos de carbono primário e secundário, com duas extremidades.
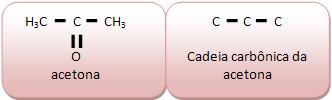
Cadeia acíclica ramificada:
Apresenta pelo menos um átomo de carbono terciário ou quaternário, com mais de duas extremidades.
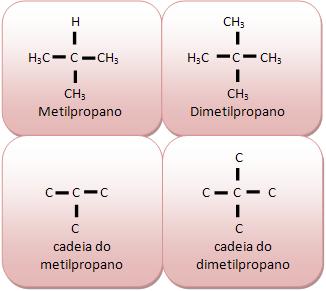
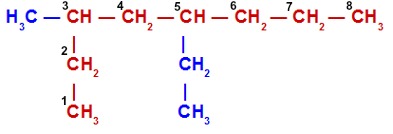
| A cadeia do composto ao lado apresenta átomos de carbono primário e secundário com três extremidades considerada ramificada.
|
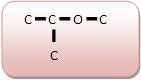
B) Quanto à natureza dos átomos
Cadeia homogênea:
Não apresenta átomos diferentes de caborno intercalados na cadeia, como as cadeias carbônicas de metilpropano e dimetilpropano, acetona e glicerol.
Cadeias heterogênea:
Apresenta átomos diferentes de carbono intercalados na cadeia. Os átomos diferentes recebem o nome de heteroátomos.
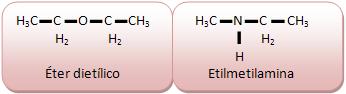
O oxigênio e o nitrogênio são considerados heteroátomos das referidas cadeias carbônicas. Somente os átomos com valência maior que 1 podem ser heteroátomos.
C) Quanto ao tipo de ligação entre os átomos de carbono
Cadeia saturada:
Os átomos de carbono ligam-se entre si, por ligações, como todas as cadeias carbônicas dos compostos mencionados até o momento.
Cadeia insaturada ou não-saturada
Apresenta uma dupla ou tripla ligação entre átomos de carbono.
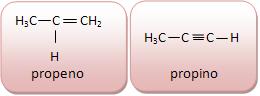
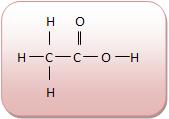
A cadeia carbônica do ácido acético é homogênea, pois entre os átomos de carbono não existe nenhum heteroátomo e na saturada entre os dois átomos de carbono existe apenas uma ligação simples. Vejamos:
III) Classificação das cadeias cíclicas ou fechadas
A) Quanto à natureza dos átomos
Cadeia homocíclica ou cíclica homogênea: em seu anel existem apenas átomos de carbono.
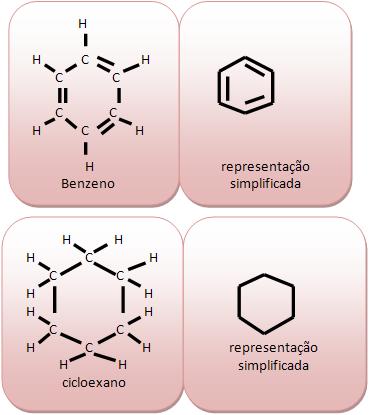
Cadeia heterocíclica ou heterogênia: em seu anel existem átomos diferentes de carbono. Vejamos:
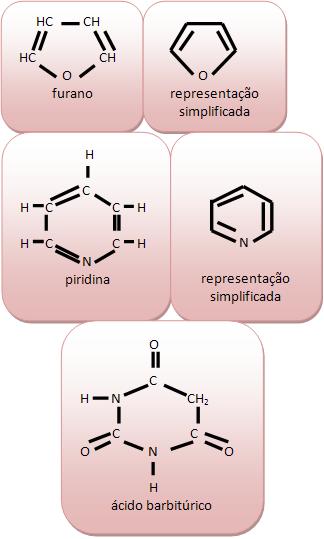
B) Classificação das cadeias homocíclicas
As cadeias homocíclicas são classificadas como cadeias alicíclicas.
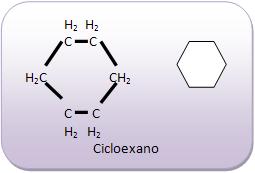
As Cadeias alicíclicas não contêm núcleo benzênico. Vejamos:
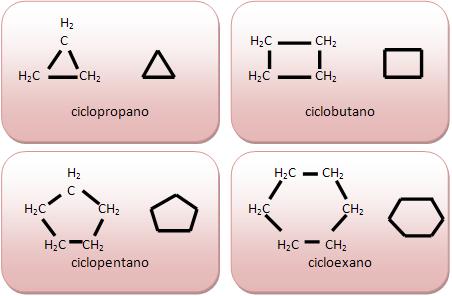
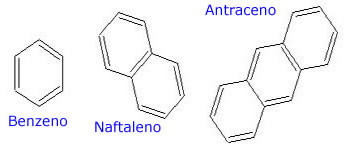
Cadeias aromáticas contêm núcleo benzênico, classificados em cadeia aromática.
O benzeno (C6H6) é um líquido incolor, que tem odor agradável, mas com vapores átoxicos, imiscíveis com água. Normalmente é usado como solvente, na fabricação de corantes, plásticos, medicamentos, explosivos. Encontrado no alcatrão de hulha, uma das frações provinientes da destilação seca da hulha, carvão mineral contendo aproximadamente 80% de carbono.
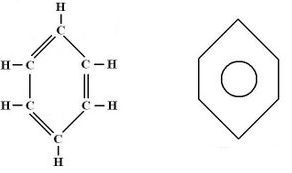
A molécula do benzeno (C6H6) é composta por seis átomos de carbono, que são ligados alternadamente, por simples e duplas ligações.
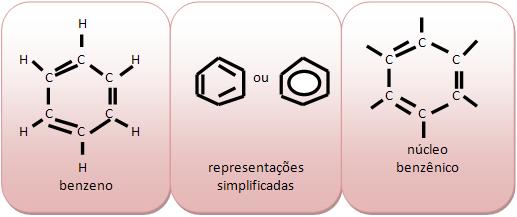
O fenol comum (C6H5OH) é considerado um sólido, pouco solúvel em água, empregado como desinfetante, na fabricação de corantes, plásticos.
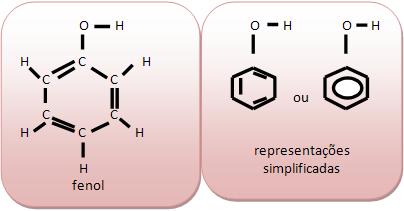
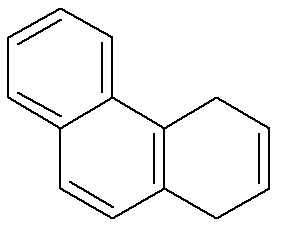
A cadeia aromática pode ser composta por mais de um núcleo benzênico.
Cadeia aromática de núcleos isolados seus anéis não possuem átomos de carbono em comum.
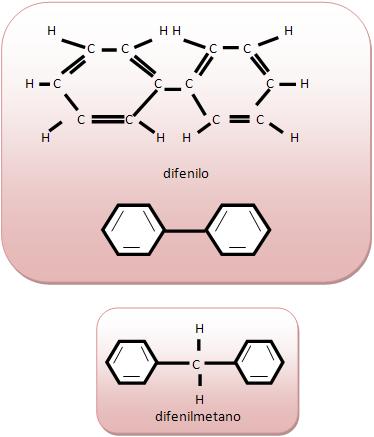
Cadeia aromática de núcleos condensados seus anéis possuem átomos de carbono comum.
Naftalleno ou naftalina (C10H8) é considerada um sólido branco que sofre sublimação para ser usado como inseticida sendo encontrado no alcatrão de hulha.
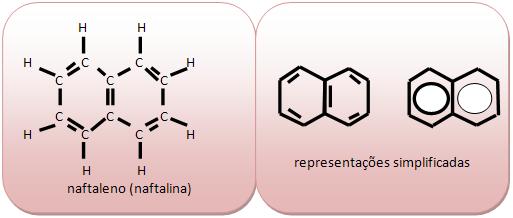
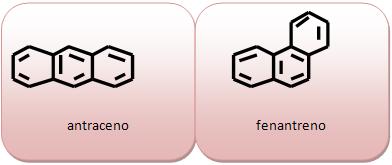
Cadeia alifática
• Existe uma certa divergência entre os autores quanto a classificação das cadeias.
• Alguns autores usam o termo cadeia alifática como sinônimo de cadeia aberta ou acíclica.
• Outros autores classificam como alifáticas as cadeias não-aromáticas.
A afirmação mais correta seria as cadeias e as alicíclicas seriam alifáticas.
Classificação das cadeias carbônicas
As cadeias carbônicas podem ser classificadas de diversas maneiras:
Quanto à disposição dos átomos de carbono
Cadeia aberta, alifática ou acíclica: é composta pelo menos de duas extremidades e não apresenta ciclos na cadeia.
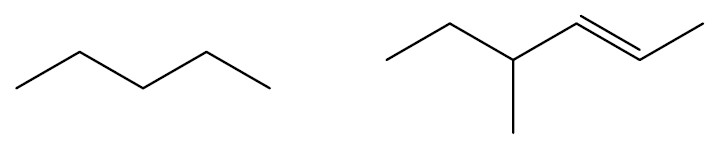
Cadeia fechada ou cíclica: não apresenta extremidades e os átomos fecham em pelo menos um ciclo.
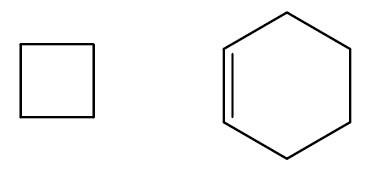
As cadeias fechadas ou cíclicas ainda se dividem em dois grupos: aromáticas e não aromáticas.
Cadeias aromáticas: possuem pelo menos um anel aromático, que é um anel que contém ligações duplas alternadas. Podem ser ramificadas ou não.
Observação:
A cadeia carbônica cíclica que contém seis átomos de carbono com três duplas ligações alternadas é denominada Aromática; esse anel chama-se Benzênico. Se a cadeia é fechada sem anel benzênico é denominada alicíclica.
Exemplo: Cadeias aromáticas:


Exemplo: Cadeias alicíclicas
As cadeias aromáticas, podem ainda, ser divididas entre mononucleares (um núcleo) ou polinucleares (mais de um núcleo). As polinucleares podem ser isoladas (núcleos não compartilham átomos) ou condensadas (núcleos compartilham átomos).
Cadeias não aromáticas ou alicíclicas: possuem uma cadeia fechada, porém que não tem as ligações duplas alternadas.
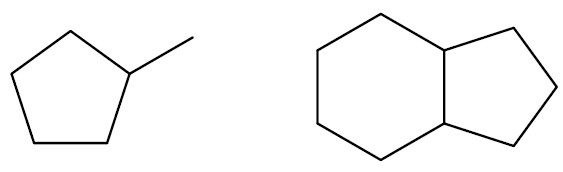
Cadeia normal ou linear: apresenta somente duas extremidades, sem ramificações.

Cadeia ramificada: apresenta no mínimo três extremidades, pois possuem ramificações.
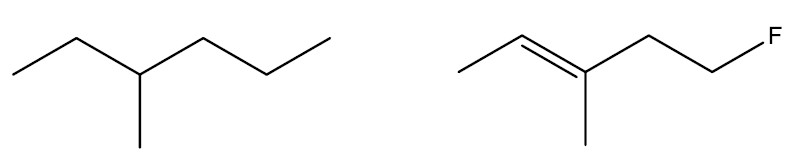
Quanto ao tipo de ligação entre os átomos de carbono
Cadeia saturada: só possui ligações simples em sua estrutura.
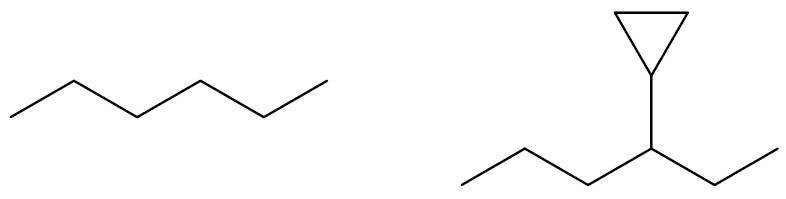
Cadeia insaturada: possui pelo menos uma ligação dupla ou tripla em sua estrutura.
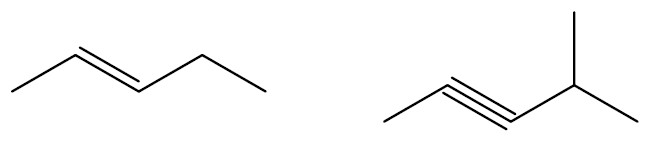
Quanto a natureza dos átomos que compõem a cadeia
Cadeia homogênea: possui apenas átomos de carbono na extensão da cadeia.
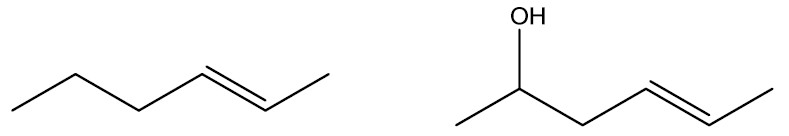
Note que a presença de um átomo diferente de carbono na ponta da cadeia não configura ela como heterogênea.
Cadeia heterogênea: possui a presença de heteroátomos.
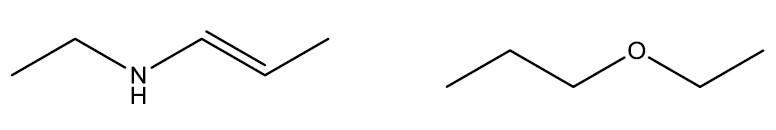
Em algumas situações, as cadeias podem ser abertas e fechadas simultaneamente, devido a presença de uma ramificação. Nestes casos, chamamos estas cadeias de mistas.
Em geral, para se classificar uma cadeia, segue-se o seguinte raciocínio:
Classificação das cadeias carbônicas fechadas
A classificação das cadeias carbônicas fechadas utiliza como referência a presença de núcleo benzênico, ligações pi ou heteroátomos.
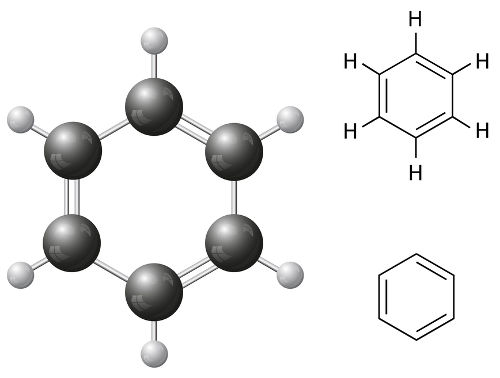 O benzeno é um dos principais exemplos de substância com cadeia carbônica fechada
O benzeno é um dos principais exemplos de substância com cadeia carbônica fechada
A classificação das cadeias carbônicas fechadas é um importante tópico estudado na química orgânica, pois, a partir desse conhecimento, é possível construir a fórmula estrutural de um composto orgânico, como ciclenos, alcoóis cíclicos, aromáticos, cetonascíclicas, éteres cíclicos, etc.
Para realizar a classificação das cadeias carbônicas fechadas, iniciamos pela divisão em dois grandes grupos:
- Cadeia carbônica fechada aromática;
- Cadeia carbônica fechada não aromática.
Classificação das cadeias carbônicas fechadas aromáticas
As cadeias fechadas aromáticas apresentam como principal característica a presença de um ciclo, que contém:
- Seis átomos de carbono;
- Seis átomos de hidrogênio;
- Um átomo de hidrogênio em cada carbono;
- 3 ligações duplas;
- 3 ligações simples;
- Ligações simples e duplas alternadas entre si.
Esse ciclo, com essas características, tem o nome oficial de benzeno. Um ponto fundamental é que ocorre no benzeno um fenômeno denominado de ressonância, no qual as ligações duplas trocam de posição de forma ininterrupta, alterando constantemente sua posição. Por essa razão, é comum simbolizar as três duplas apenas por um círculo, que representa a ressonância.
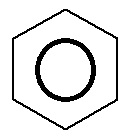
Fórmula estrutural do benzênico com o anel
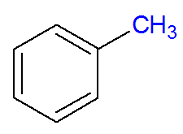
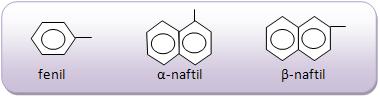
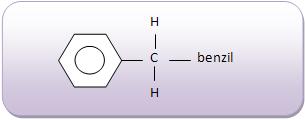
a) Aromáticas mononucleares
São as cadeias aromáticas que apresentam apenas um benzeno, que está ligado a outro elemento (por exemplo, o cloro), grupo substituinte (como o radical metil, CH3) ou um grupo funcional (como a carboxila).
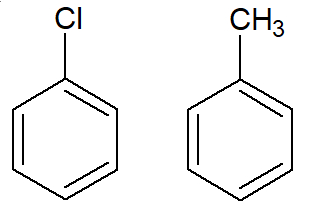
Exemplos de aromáticos mononucleares
b) Aromáticas polinucleares
- Com núcleos isolados
Nesse tipo de cadeia carbônica aromática, há a presença de dois ou mais núcleos benzênicos, porém separados por um átomo de um elemento (por exemplo, um oxigênio) ou grupo funcional (por exemplo, a carbonila de uma cetona).
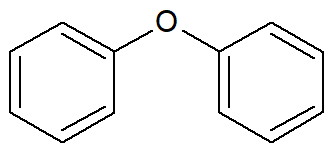
Fórmula estrutural de um aromático isolado por um elemento químico
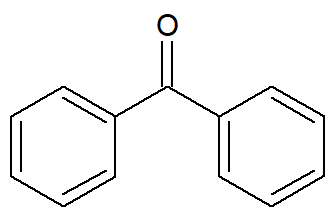
Fórmula estrutural de um aromático isolado por um grupo funcional de cetona
- Com núcleos condensados
Nesse tipo de cadeia carbônica fechada aromática, temos a presença de dois ou mais núcleos benzênicos, unidos entre si, ou seja, existem carbonos e ligações em comum nas estruturas.
As cadeias aromáticas podem ser classificadas de acordo com o número de anéis aromáticos:
– mononuclear: quando possui apenas um núcleo (anel aromático)
– polinuclear: quando possui vários anéis aromáticos.
Os aromáticos polinucleares podem ser classificados em:
– polinucleares isolados: quando os anéis não possuem átomo de carbono em comum.
– polinuclear condensado: quando os anéis possuem átomos de carbono em comum.
- Cadeia carbônica fechada não aromática.
– saturada: cadeia que possui apenas ligações simples entre os átomos.
– insaturada: cadeia que possui uma dupla ligação entre carbonos.
Podem ser classificadas de acordo com a presença ou não de um heteroátomo:
– homogênea ou homocíclicas: possuem somente átomos de carbonos ligados entre si.
– heterogênea ou heterocíclica: possuem um heteroátomo entre átomos de carbono.
Cadeias mistas
As cadeias carbônicas mistas são abertas e também fechadas.
Lista de Exercícios – cadeias carbônicas
Classifique as cadeias existentes em cada uma das estruturas a seguir e determine o número de carbonos primários, secundários, terciários e quaternários, e escreva suas fórmulas moleculares :
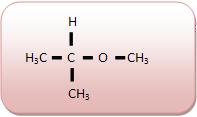
1 – (Padre Anchieta SP) A substância de fórmula CH3–O–CH2–CH3 tem cadeia carbônica:
a) acíclica, homogênea e normal.
b) cíclica, heterogênea e ramificada.
c) cíclica, homogênea e saturada.
d) acíclica, insaturada e heterogênea.
e) acíclica, saturada e heterogênea.
2 – . (Unifor CE) A acrilonitrila, H2C=CH–CN, matéria-prima usada na obtenção de fibras têxteis, tem cadeia carbônica:
a) acíclica e ramificada.
b) cíclica e insaturada.
c) cíclica e ramificada.
d) aberta e homogênea.
e) aberta e saturada.
3 – (UFRN) A cadeia carbônica acíclica, ramificada, homogênea e insaturada é:
![]()


![]()

4- (MACK SP) O hidrocarboneto, que apresenta a menor cadeia carbônica aberta, saturada e ramificada, tem fórmula molecular:
a) CH4
b) C4H8
c) C5H8
d) C4H10
e) C2H4
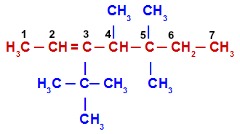
5 – (ITE SP) O composto orgânico, de fórmula plana, possui:

a) 5 carbonos primários, 3 carbonos secundários, 1 carbono terciário e 2 carbonos quaternários.
b) 3 carbonos primários, 3 carbonos secundários, 1 carbono terciário e 1 carbono quaternário.
c) 5 carbonos primários, 1 carbono secundário, 1 carbono terciário e 1 carbono quaternário.
d) 4 carbonos primários, 1 carbono secundário, 2 carbonos terciários e 1 carbono quaternário.
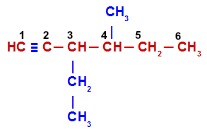
6 – (MACK SP) O composto apresenta:

a) cadeia carbônica insaturada.
b) somente carbonos primários.
c) um carbono quaternário.
d) três carbonos primários e um terciário.
e) cadeia carbônica heterogênea.
7 – (UFJF MG) Classificar a cadeia da molécula 3-metil 1-penteno.
a) cíclica, ramificada, saturada, homogênea;
b) acíclica, normal, insaturada, heterogênea;
c) acíclica, ramificada, insaturada, homogênea;
d) cíclica, ramificada, saturada, homogênea;
e) acíclica, ramificada, saturada, homogênea;
8- (UEL PR) Dentre os componentes do cigarro, encontram-se a nicotina que interfere no fluxo de informações entre as células, a amônia que provoca irritação nos olhos e o alcatrão, formado pela mistura de compostos como o benzopireno, o crizeno e o antraceno, todos com potencial cancerígeno.
Sobre o benzopireno, cuja estrutura química é apresentada a seguir, é correto afirmar que a molécula é formada por:

a) Cadeias aromáticas com núcleo benzênico.
b) Arranjo de cadeias carbônicas acíclicas.
c) Cadeias alicíclicas de ligações saturadas.
d) Cadeias carbônicas heterocíclicas.
e) Arranjo de anéis de ciclohexano.
9. O náilon é um polímero de condensação, mais especificamente da classe das poliamidas, que são polímeros formados pela condensação de um diácido carboxílico com uma diamida. Uma das variedades desse polímero pode ser obtida por meio de uma matéria-prima denominada de caprolactana, cuja fórmula estrutural é:
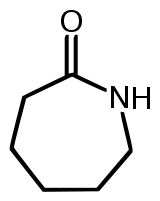
Fórmula da caprolactana
Analisando essa cadeia, podemos classificá-la em:
a) Fechada, insaturada, heterogênea, mononuclear.
b) Alicíclica, insaturada, heterogênea, mononuclear.
c) Fechada alicíclica, saturada, heterogênea, mononuclear.
d) Fechada alicíclica, insaturada, homogênea, mononuclear.
e) Fechada, insaturada, homogênea, mononuclear.
10. Considere as seguintes substâncias, suas fórmulas estruturais e aplicações:
1. Cl — CH2 — S — CH2 — CH2 — Cl→ gás mostarda
2. HS — CH2 — CH — CH2 — OH → antídoto no envenenamento por arsênio
|
SH
CH3
|
3. H3C — CH — CH2 — CH2 — SH → cheiro desagradável do gambá
4..jpg) → anestésico
→ anestésico
5. 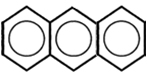 → Substância presente na fumaça do cigarro
→ Substância presente na fumaça do cigarro
Molécula de antraceno
O
||
6. H3C — CH2 — CH2 — C — O — CH2 — CH3 → essência de abacaxi
Qual(is) dentre essas cadeias carbônicas pode(m) ser classificada (s) como uma cadeia alifática, normal, saturada e heterogênea?
a) 1, 2, 3, 6.
b) Todas.
c) 4,5.
d) 1 e 6.
e) Somente 1.
11. UFAM-PSC) O pau-rosa, típico da região amazônica, é uma rica fonte natural do óleo essencial conhecido por linalol, o qual também pode ser isolado do óleo de alfazema. Esse óleo apresenta a seguinte fórmula estrutural:
OH
|
H3C — C = CH — CH2 — CH2 — C — CH = CH2
| |
CH3 CH3
Sua cadeia carbônica deve ser classificada como:
a) acíclica, ramificada, saturada e heterogênea.
b) acíclica, normal, insaturada e homogênea.
c) alicíclica, ramificada, insaturada e homogênea.
d) acíclica, ramificada, insaturada e homogênea.
e) alicíclica, normal, saturada e heterogênea.
12. (PUC-RS) O ácido etilenodiaminotetracético, conhecido como EDTA, utilizado como antioxidante em margarinas, de fórmula
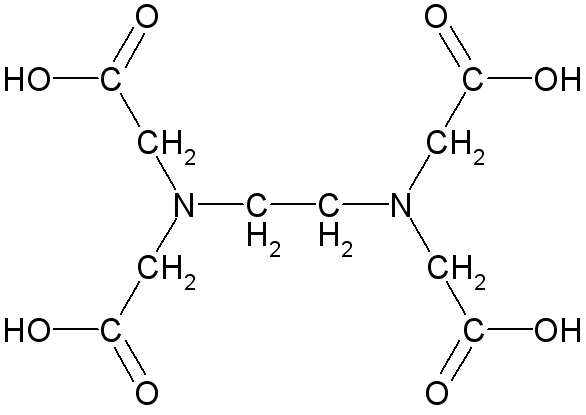
Fórmula do EDTA (ácido etilenodiaminotetracético)
Apresenta cadeia carbônica
a) acíclica, insaturada, homogênea.
b) acíclica, saturada, heterogênea.
c) acíclica, saturada, homogênea.
d) cíclica, saturada, heterogênea.
e) cíclica, insaturada, homogênea.



.jpg)








.jpg)



.jpg)
.jpg)