Conteúdos e temas: ligação química; modelo explicativo para a transformação química; energia de ligação; modelo explicativo para transformações químicas exotérmicas e endotérmicas.
Competências e habilidades: empregar a linguagem química; interpretar a transformação química como
a quebra e formação de ligações; compreender e identificar a energia envolvida na quebra e formação de
ligações químicas; fazer previsões a respeito da energia envolvida numa transformação química.
Estratégias de ensino: aula expositiva dialogada; resolução de problemas; trabalho individual.
Recursos: texto; materiais de laboratório; roteiro experimental.
Avaliação: respostas às questões.
Ligação covalente
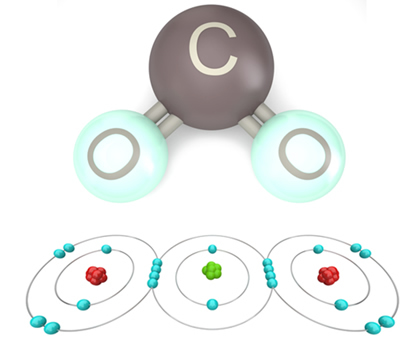
A ligação covalente é um tipo de ligação química que ocorre entre átomos de hidrogênio, ametais e semimetais, com a finalidade de ficarem estáveis. A estabilidade eletrônica é alcançada quando o átomo fica com oito elétrons na sua camada de valência (última camada eletrônica), ficando com a configuração de um gás nobre, sendo que a única exceção é o hidrogênio, que fica estável com apenas dois elétrons.
Portanto, todos os átomos dos elementos mencionados (hidrogênio, ametais e semimetais) possuem a tendência de receber elétrons para ficarem estáveis. Visto que não é possível que todos recebam elétrons, senão pelo menos um não ficaria estável, então os átomos envolvidos na ligação covalente compartilham um ou mais pares de elétrons.
Veja como isso ocorre:
Uma molécula de cloreto de hidrogênio (HCl) é formada por uma ligação covalente entre um átomo de hidrogênio e um átomo de cloro.
Conforme se pode ver abaixo, o átomo do hidrogênio possui somente um elétron na sua camada eletrônica, precisando receber mais um elétron para ficar estável:
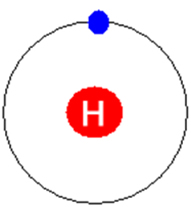
Átomo de hidrogênio
Por outro lado, o cloro possui 17 elétrons no estado fundamental, sendo que, na sua camada de valência, ele tem sete elétrons. Isso significa que ele precisa receber mais um elétron para ficar estável:
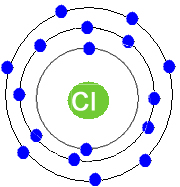
Átomo de cloro
Assim, visto que tanto o hidrogênio quanto o cloro precisam receber um elétron, eles compartilham um par de elétrons, ficando ambos estáveis:
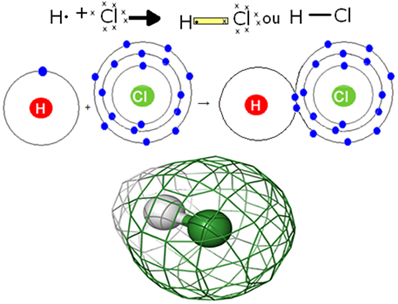
Formação do cloreto de hidrogênio por ligação covalente
Veja que se formou uma molécula. Isso sempre acontece nas ligações covalentes, ou seja, formam-se unidades isoladas e de grandeza limitada. Por isso, as ligações covalentes também são chamadas de moleculares.
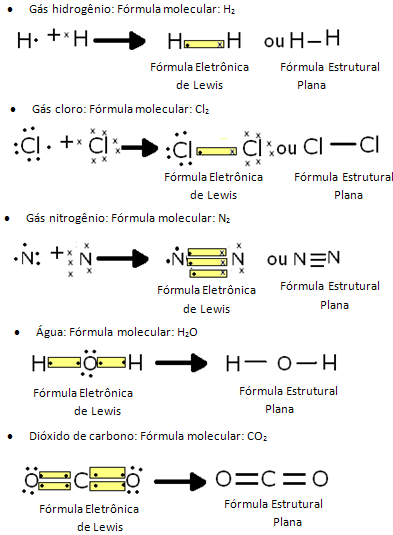
Esse tipo de ligação pode ocorrer entre átomos diferentes, como no exemplo do HCl, ou entre átomos de um mesmo elemento, como os exemplos abaixo. Ao analisá-los, observe que essa maneira de representar a ligação, em que se representam os elétrons da camada eletrônica por bolinhas ou “x”, é conhecida como fórmula eletrônica de Lewis.
Outra forma de representar esse tipo de ligação mostrada abaixo é a fórmula estrutural plana, em que cada par de elétrons compartilhados é simbolizado por um traço:
Ligação covalente dativa
A ligação covalente dativa ocorre quando um átomo transfere elétrons, essa transferência é indicada pelo vetor (seta).
Ligação covalente dativa ocorre quando um átomo compartilha seus elétrons. Essa ligação obedece à Teoria do Octeto, onde os átomos se unem tentando adquirir oito elétrons na camada de valência para atingir a estabilidade eletrônica.Exemplo: formação de dióxido de enxofre (SO2)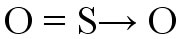 O átomo de enxofre (S) adquire seu octeto através da ligação com o oxigênio localizado à esquerda (ligação dupla coordenada). O oxigênio à direita necessita de elétrons para completar a camada de valência, e então o enxofre doa um par de elétrons para esse oxigênio. Essa transferência de elétrons é indicada pelo vetor (seta) e corresponde à ligação covalente dativa.Vejamos o compartilhamento de elétrons na formação do composto Sulfato, onde um átomo central de enxofre estabelece ligações covalentes com quatro átomos de oxigênio.
O átomo de enxofre (S) adquire seu octeto através da ligação com o oxigênio localizado à esquerda (ligação dupla coordenada). O oxigênio à direita necessita de elétrons para completar a camada de valência, e então o enxofre doa um par de elétrons para esse oxigênio. Essa transferência de elétrons é indicada pelo vetor (seta) e corresponde à ligação covalente dativa.Vejamos o compartilhamento de elétrons na formação do composto Sulfato, onde um átomo central de enxofre estabelece ligações covalentes com quatro átomos de oxigênio.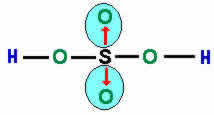 As setas vermelhas indicam as ligações dativas e os traços indicam o compartilhamento de elétrons. Na ligação dativa, o átomo de enxofre “doa” um par de elétrons para cada átomo de oxigênio, estes, por sua vez, atingem a estabilidade eletrônica.
As setas vermelhas indicam as ligações dativas e os traços indicam o compartilhamento de elétrons. Na ligação dativa, o átomo de enxofre “doa” um par de elétrons para cada átomo de oxigênio, estes, por sua vez, atingem a estabilidade eletrônica.
Exemplos de ligações covalentes
Aproveite para conferir nossas videoaulas relacionadas ao assunto:


