Distribuição Eletrônica
Linus Pauling foi o criador de um diagrama que facilitou a distribuição dos elétrons dos átomos nos níveis e subníveis eletrônicos
modelo atômico de Rutherford-Böhr mostra que o átomo possui um núcleo com prótons e nêutrons, além de uma eletrosfera formada por várias camadas eletrônicas, com valores de energia específicos para cada tipo de átomo. Para os elementos conhecidos atualmente, existem, no máximo, sete camadas que são representadas, respectivamente (de dentro para fora), pelas letras K, L, M, N, O, P e Q.
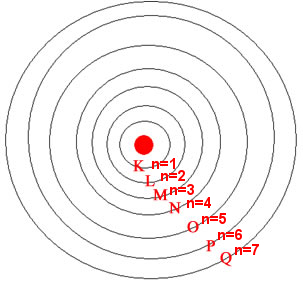
Sete camadas eletrônicas representadas pelas letras
A distribuição eletrônica refere-se ao modo em que os elétrons estão distribuídos nas camadas ou níveis de energia que ficam ao redor do núcleo do átomo. Por exemplo, abaixo temos os elétrons do berílio. Ele possui 4 elétrons no total, distribuídos em duas camadas eletrônicas. Assim, a sua distribuição eletrônica é dada por: 2 – 2.
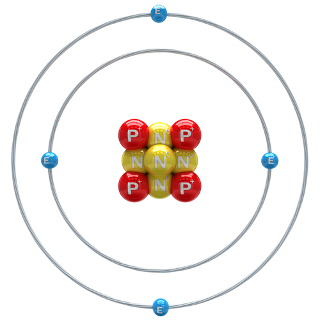
Átomo de berílio
Distribuição Eletrônica
Camadas Eletrônicas ou Níveis de Energia
A coroa ou eletrosfera está dividida em 7 camadas designadas por K, L, M, N, O, P, Q ou pelos números: n = 1, 2, 3, 4, 5, 6, 7.
O número de camada é chamado número quântico principal (n).
Número máximo de elétrons em cada nível de energia:
1. Teórico:
Equação de Rydberg: x = 2n2
| K | L | M | N | O | P | Q |
| 2 | 8 | 18 | 32 | 50 | 72 | 98 |
- Experimental:
O elemento de número atômico 112 apresenta o seguinte número de elétrons nas camadas energéticas:
| K | L | M | N | O | P | Q |
| 2 | 8 | 18 | 32 | 32 | 18 | 2 |
No entanto, os elétrons não se distribuem de qualquer forma nessas camadas, havendo, portanto, algumas regras a serem seguidas para essa distribuição. Por exemplo, a primeira camada (K) suporta no máximo 2 elétrons, e a camada de valência (a última camada a ser preenchida) pode possuir no máximo 8 elétrons.
Esses e outros fatores ocorrem porque os elétrons distribuem-se nas camadas eletrônicas de acordo com subníveis de energia, que são identificados pelas letras s, p, d, f, que aumentam de energia nessa ordem respectiva. Cada nível comporta uma quantidade máxima de elétrons distribuídos nos subníveis de energia.
Antes de você poder realizar a distribuição eletrônica de um átomo por meio do Diagrama de Pauling, é necessário saber qual a quantidade máxima de elétrons que pode ser distribuída em cada nível e subnível. Isso está evidenciado a seguir:
Camada de valência é a camada mais externa do átomo e pode contar no máximo 8 elétrons
Subcamadas ou Subníveis de Energia
Uma camada de número n será subdividida em n subníveis:
s, p, d, f, g, h, i…
Nos átomos dos elementos conhecidos, os subníveis teóricos g, h, i… estão vazios.
Número máximo de elétrons em cada subnível experimental:
s p d f
2 6 10 14
Distribuição dos elétrons nos subníveis (configuração eletrônica)
Os subníveis são preenchidos em ordem crescente de energia (ordem energética). Linus Pauling descobriu que a energia dos subníveis cresce na ordem:
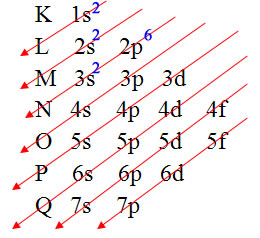
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d…
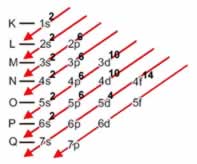
Para tornar mais fácil a distribuição dos elétrons dos átomos nas camadas eletrônicas, o cientista Linus Pauling (1901-1994) criou uma representação gráfica que facilitou a visualização da ordem crescente de energia e a realização da distribuição eletrônica. Essa representação passou a ser chamada de Diagrama de Pauling, sendo também conhecida como Diagrama de distribuição eletrônica ou, ainda, Diagrama dos níveis energéticos, e está exposta abaixo:

A representação gráfica da distribuição eletrônica é dada pelo Diagrama de Pauling
Seqüência de preenchimento de orbitais
Deve-se observar a ordem energética dos subníveis de energia, que infelizmente não é igual à ordem geométrica. Isso porque subníveis de níveis superiores podem ter menor energia total do que subníveis inferiores.
A energia de um subnível é proporcional à soma (n + l) de seus respectivos números quânticos principal (n) e secundário (l).
O número quântico azimutal ou secundário, representado pela letra l, especifica a subcamada e, assim, a forma do orbital. Pode assumir os valores 0, 1, 2 e 3, correspondentes às subcamadas s, p, d, f.
Método analítico para ordenação dos subníveis:
Exemplos
1) 3d 4s
n = 3 n = 4
l = 2 l = 0
n + l = 5 n + l = 4
3d é mais energético que 4s
2) 3d 4p
n = 3 n = 4
l = 2 l = 1
n + l = 5 n + l = 5
Quando os subníveis apresentarem a mesma soma, o mais afastado ou de maior nível energético terá maior energia.
Ordem geométrica é a ordenação crescente de níveis energéticos.
Exemplo: 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p…
Camada de Valência é o último nível de uma distribuição eletrônica, normalmente os elétrons pertencentes à camada de valência, são os que participam de alguma ligação química.
Exemplo: Arsênio (As): Z = 33
– Ordem energética (ordem de preenchimento): 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p3
– Ordem geométrica (ordem de camada): 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p3
Camadas Energéticas: K = 2; L = 8; M = 18; N = 5
A camada de valência do As é a camada N, pois é o último nível que contém elétrons.
Distribuição Eletrônica em Íons
Átomo: nº de prótons = nº de elétrons
Íon: nº de prótons (p) ≠ nº de elétrons
Íon positivo (cátion): nº de p > nº de elétrons
Íon negativo (ânion): nº de p < nº de elétrons
Distribuição Eletrônica em Cátion
Retirar os elétrons mais externos do átomo correspondente. Exemplo:
Ferro (Fe) Z = 26 → 1s2 2s2 2p6 3s2 3p6 4s2 3d6 (estado fundamental = neutro)
Fe2+ → 1s2 2s2 2p6 3s2 3p6 3d6 (estado iônico)
Distribuição Eletrônica em Ânion
Colocar os elétrons no subnível incompleto. Exemplo:
Oxigênio (O) Z = 8 → 1s2 2s2 2p4 (estado fundamental = neutro)
O2- → 1s2 2s2 2p6
Os números átomos.
Existem quatro números quânticos:quânticos descrevem a posição (e a energia) dos elétrons nos
número quântico principal: indica o nível (camada) de energia.
número quântico secudário ou azimutal: indica o sub-nível de energia.
número quântico magnético: indica o orbital.
número quântico de spin: indica a orientação do elétron no orbital.
Dois elétrons nunca terão os quatro números quânticos iguais, pois mesmo que estejam no mesmo nível, no mesmo sub-nível e no mesmo orbital, terão spins opostos. Assim, qualquer par de elétrons pode ter até três números quânticos iguais.
- Número quântico principal, n
O número quântico principal terá como valores 1, 2, 3, 4…de acordo com o nível eletrônico que o elétron se encontra.
- Número quântico azimutal, l
O número quântico azimutal, informa-nos sobre a forma dos orbitais (s, p, d, f). Para um dado valor de n, l pode ter como valores possíveis os números inteiros de 0 a (n − 1). Para os sub-níveis s, p d, f, temos:
s = 0, p = 1 , d = 2 , f = 3
- Número quântico magnético, ml
O número quântico magnético especifica a orientação permitida para uma nuvem eletrônica no espaço, sendo que o número de orientações permitidas está diretamente relacionado à forma da nuvem (designada pelo valor de l). Dessa forma, este número quântico pode assumir valores inteiros de -l, passando por zero, até +l. Para os sub-níveis s, p d, f, temos:
| s | 0 | ||||||
| p | -1 | 0 | +1 | ||||
| d | -2 | -1 | 0 | +1 | +2 | ||
| f | -3 | -2 | -1 | 0 | +1 | +2 | +3 |
- Número quântico de spin, ms
O número quântico de spin indica a orientação do elétron ao redor do seu próprio eixo. Como existem apenas dois sentidos possíveis, este número quântico assume apenas os valores -1/2 e +1/2.
- Exemplos: Quais os nºs quânticos do último elétron (elétron diferencial, verificador) de cada átomo abaixo?Al = 1s22s22p63s23p1
Logo os nºs quânticos são referentes ao elétron de 3p1:
n = 3 (terceiro nível)
l = 1 (sub-nível p)
ml = -1 (primeiro orbital p)
ms = -1/2 (rotação)
Fe = 1s22s22p63s23p64s23d6
Logo os nºs quânticos são referentes ao elétron de 3d6:
n = 3 (terceiro nível)
l = 2 (sub-nível d)
ml = -2 (primeiro orbital d)
ms = +1/2 (rotação)
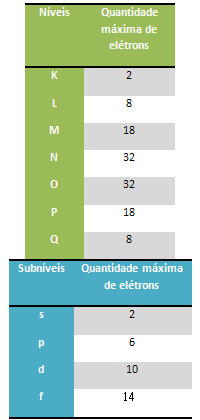
Quantidade máxima de elétrons para preencher cada nível e subnível
Além disso, lembre-se de que os elétrons vão preenchendo esses subníveis de acordo com a ordem crescente de energia, que, no Diagrama de Pauling, é dada pelo sentido das setas.
Agora sim, vejamos um exemplo de como aplicar esses conceitos na distribuição eletrônica:
Exemplo 1: Vamos realizar a distribuição eletrônica do magnésio (Mg), cujo número atômico (Z – número de prótons) é igual a 12.
Visto que está no estado fundamental, a quantidade de elétrons e de prótons é igual, ou seja, temos que distribuir 12 elétrons.
Começaremos pelo subnível 1s, onde só cabem 2 elétrons, e continuaremos preenchendo e seguindo as setas até completar 12 elétrons:
Distribuição eletrônica do magnésio no diagrama de Pauling
Observe que a distribuição eletrônica do magnésio em subníveis de energia é dada por: 1s2 2s2 2p6 3s2.
Já a distribuição eletrônica por camadas foi: 2 – 8 – 2, ou seja, o átomo desse elemento possui 2 elétrons na camada K, 8 elétrons na camada L e 2 dois elétrons na camada M.
Entendeu como se faz a distribuição eletrônica no diagrama de Pauling?
Veja mais dois exemplos para tirar suas dúvidas:
Exemplo 2: Vanádio (Z = 23)
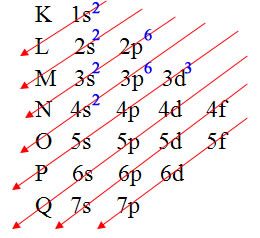
Distribuição eletrônica do vanádio no diagrama de Pauling
- Ordem energética: 1s2 2s2 2p6 3s2 3p6 4s2 3d3
- Ordem geométrica: 1s2 2s2 2p6 3s2 3p6 3d3 4s2
- Número total de elétrons por nível ou camada: K = 2, L = 8, M = 11, N = 2
- Número de elétrons no subnível mais energético: o subnível mais energético é o último a ser preenchido, isto é, o 3d. Assim, o número de elétrons nele é 3.
- Número de elétrons no subnível mais externo: o subnível mais externo é o que fica mais afastado do núcleo, isto é, o 4S. Assim, o número de elétrons nele é 2.
Exemplo 3: Bário (Z = 56)
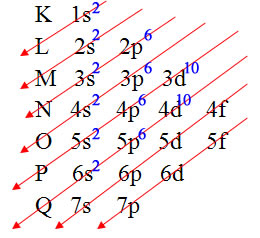
Distribuição eletrônica do bário no diagrama de Pauling
- Ordem energética: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2
- Ordem geométrica: 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 6s2
- Número total de elétrons por nível ou camada: K = 2, L = 8, M = 18, N = 18, O = 8, P = 2.
- Número de elétrons no subnível mais energético: o subnível mais energético é o 6s. Assim, o número de elétrons nele é 2.
- Número de elétrons no subnível mais externo: o subnível mais externo também é o 6s. Assim, o número de elétrons nele é 2.
Aproveite para conferir nossas videoaulas sobre o assunto:
Números Quânticos
Home / Química Geral / Números Quânticos

O Princípio da Incerteza de Werner Heisenberg (1901-1976), criado em 1926, estabeleceu que não é possível calcular a posição e a velocidade de um elétron em um mesmo instante, ou seja, quanto maior for a precisão da determinação da medida da posição do elétron, menor será a precisão da medida de sua velocidade e vice-versa.
Por isso, os cientistas passaram a adotar o conceito de “orbital”, que se refere à região no espaço ao redor do núcleo do átomo onde é maior a probabilidade de se encontrar determinado elétron. No modelo de orbitais, o elétron tem característica dual, isto é, como onda-partícula que se desloca no espaço, mas que está dentro de uma região (orbital) ao redor do núcleo, como uma nuvem eletrônica.
Esse movimento do elétron passou a ser descrito por Erwin Schrödinger por meio de uma equação matemática que associava a natureza corpuscular do elétron, ou seja, sua natureza como partícula, sua energia, carga e massa.
Durante o processo algébrico da solução da equação de Schrödinger, surgiram naturalmente códigos matemáticos relacionados com a energia do elétron, que são denominados de números quânticos.Existem quatro números quânticos: número quântico principal (n), número quântico secundário ou azimutal (l), número quântico magnético (m ou ml) e número quântico spin (s ou ms).
O conjunto de números quânticos nunca se repete para dois elétrons em um átomo. Portanto, esse conjunto de números quânticos serve para identificar cada elétron na eletrosfera de um átomo. Então, vejamos como determinar cada um:
1. Número quântico principal (n): Refere-se ao nível de energia do elétron.
Segundo o modelo atômico de Rutherford-Bohr, os elétrons movimentam-se ao redor do núcleo em órbitas circulares com quantidades de energia bem definidas e características, sendo, portanto, chamadas de níveis de energia ou camadas eletrônicas. Para os elementos conhecidos até o momento, a quantidade máxima de níveis de energia são sete, sendo representados pelas letras K, L, M, N, O, P e Q, indo da camada mais próxima ao núcleo para a mais distante. Essas camadas correspondem respectivamente aos números 1, 2, 3, 4, 5, 6 e 7.
Assim, os valores de n variam de 1 a 7, de acordo com o nível de energia do elétron. Quanto maior o número quântico principal, maior é a energia do elétron.
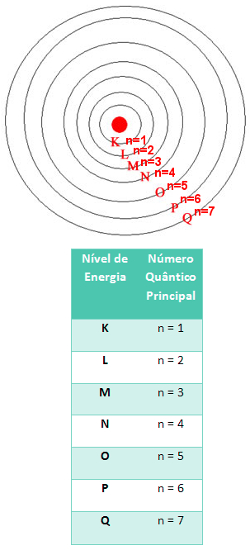
Relação entre o nível de energia e o número quântico principal
2. Número quântico secundário ou azimutal (l): Refere-se ao subnível de energia do elétron.
Conforme explicado no texto Distribuição eletrônica, os elétrons distribuem-se nas camadas eletrônicas de acordo com subníveis de energia, que são identificados pelas letras s, p, d, f, que aumentam de energia nessa ordem. Cada nível comporta uma quantidade máxima de elétrons distribuídos nos subníveis de energia.
Para os elementos até então conhecidos, temos apenas quatro tipos de subníveis:
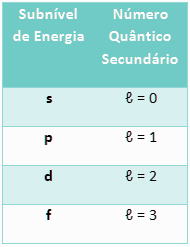
Tabela da relação entre o subnível de energia e o número quântico secundário
Isso significa que, para um número quântico principal n, o número quântico secundário será l = n – 1.
3. Número quântico magnético (m ou ml): Refere-se à orientação dos orbitais no espaço.
O orbital do tipo s possui forma esférica e, portanto, só há uma orientação possível para ele. Desse modo, só haverá um valor possível para o número quântico magnético, que será igual a 0:
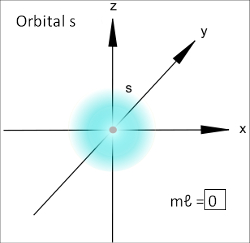
Representação do orbital s
Veja que o orbital é representado por um quadrado.
Em relação ao subnível do tipo p, conforme a figura abaixo indica, existem três orientações espaciais possíveis, porque ele apresenta-se na forma de um duplo ovoide. Então, para o subnível p, há três números magnéticos possíveis, -1, 0, +1, que são representados por três quadradinhos:
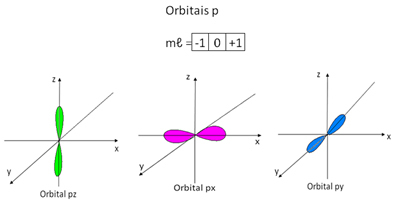
Representação dos orbitais p
Já o subnível d possui cinco orientações espaciais possíveis, sendo que o número magnético pode apresentar os seguintes valores: -2, -1, 0, +1, +2:
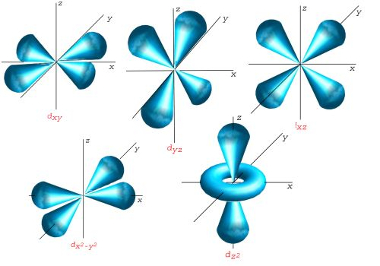
Representação dos orbitais d
Por fim, o subnível f possui sete orientações espaciais possíveis, sendo que o número magnético pode apresentar os seguintes valores: -3, -2, -1, 0, +1, +2, +3:

Representação dos orbitais f*
Desse modo, temos as seguintes possibilidades:
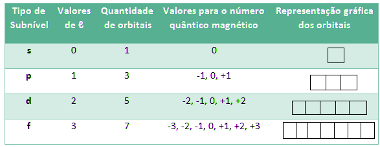
Tabela da relação entre orbitais e o número quântico magnético
Esses orbitais costumam ser representados de acordo com um diagrama energético, como o mostrado a seguir, em que cada “escada” corresponde ao nível e cada “degral” corresponde ao subnível.
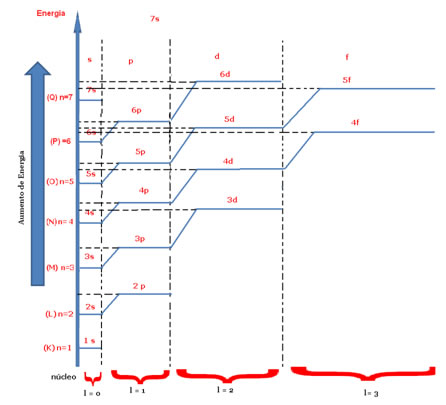
Diagrama energético indicando o número quântico magnético
4. Número quântico spin (s ou ms): Refere-se ao sentido da rotação (no inglês, spin significa rotação) do elétron.
Dois elétrons conseguem ficar em um mesmo orbital e não se repelirem porque eles giram em sentidos opostos, o que causa uma força magnética de atração. Assim, o magnetismo em razão do spin de um elétron é anulado pelo magnetismo do spin oposto, ficando um sistema estável.
É por isso que cada orbital possui no máximo dois elétrons com spins opostos, que são simbolizados por setas. Isso é dito pelo Princípio da Exclusão de Pauli.
Por convenção, adotamos o seguinte: a seta para cima corresponde a ms= -1/2, e a seta para baixo corresponde a ms= +1/2.
ms = -1/2 ou +1/2
ms = ↑ ou ↓
Segundo a Regra de Hund ou Regra de máxima multiplicidade, o preenchimento dos orbitais de um subnível deve ser feito de uma forma que contenha o maior número possível de elétrons desemparelhados (isolados). Por isso, temos que preencher primeiro os orbitais (quadradinhos), colocando somente as setas para cima, e depois voltamos preenchendo as setas para baixo.
Vejamos um exemplo:
Indique os quatro números quânticos para o elétron mais energético do Cobre (Z = 29):
Resolução:
Primeiro realizamos a distribuição eletrônica no Diagrama de Pauling dos 29 elétrons do cobre:
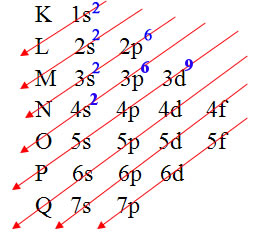
Distribuição eletrônica do cobre no diagrama de Pauling
Veja que o subnível mais energético é o último a ser preenchido, ou seja, o 3d9.
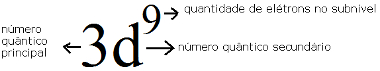
Subnível mais energético do cobre e sua relação com os números quânticos
*O nível é o M, ou seja, o número principal é: n =3.
*O subnível é o d, então, o número quântico secundário é: l = 2.
* Visto que são nove (9) elétrons e queremos saber o do nono elétron, que foi o último a ser preenchido e que é o mais energético, vamos realizar a distribuição deles nos orbitais para descobrir o número quântico magnético e o spin. Lembrando que primeiro vamos preencher com todas as setas para cima e depois preencher com as setas para baixo:
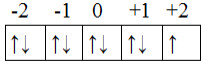
Distribuição eletrônica nos orbitais do subnível mais energético do cobre
A última seta a ser preenchida, que é o elétron mais energético, ficou no +1, então, o valor do número quântico magnético é: ml = +1.
*Visto que a seta está para baixo, por convenção, adotamos que o número quântico spin é: ms = +1/2.
* Crédito da imagem: Autor: CK-12 Foundation/ Extraído de: Wikimedia Commons.
QUÍMICA-DIAGRAMA DE LINUS PAULING
1) Utilizando o diagrama de Pauling, realize a distribuição eletrônica do elemento tungstênio (W), cujo número atômico (Z) é igual a 74 e, posteriormente, forneça:
a) A distribuição eletrônica em ordem de energia;
b) A ordem geométrica;
c) O número total de elétrons por camada;
d) O número de elétrons no subnível mais energético;
e) O número de elétrons no subnível mais externo.
2) Faça a distribuição eletrônica em níveis de energia para os seguintes elementos:
a) 9F
b) 10Ne
c) 15P
d) 28Ni
e) 56Ba
3) (UNI-RIO)“Os implantes dentários estão mais seguros no Brasil e já atendem às normas internacionais de qualidade. O grande salto de qualidade aconteceu no processo de confecção dos parafusos e pinos de titânio, que compõem as próteses. Feitas com ligas de titânio, essas próteses são usadas para fixar coroas dentárias, aparelhos ortodônticos e dentaduras, nos ossos da mandíbula e do maxilar.”
Jornal do Brasil, outubro 1996.
Considerando que o número atômico do titânio é 22, sua configuração eletrônica será:
a) 1s22s22p6 3s2 3p3
b) 1s22s22p6 3s2 3p5
c) 1s22s22p6 3s2 3p6 4s2
d) 1s22s22p6 3s2 3p6 4s2 3d2
e) 1s22s22p6 3s2 3p6 4s2 3d10 4p6
4) Considerando-se um elemento M genérico qualquer, que apresenta configuração eletrônica 1s2 2s2 2p6 3s2 3p6 4s2 3d5, pode-se afirmar que:
- seu número atômico é 25;
- possui 7 elétrons na última camada;
III. apresenta 5 elétrons desemparelhados;
- pertencem a família 7A.
Estão corretas as afirmações:
a) I, II e III somente
b) I e III somente
c) II e IV somente
d) I e IV somente
e) II, III e IV somente
5) (UFSC) O número de elétrons em cada subnível do átomo estrôncio (38Sr) em ordem crescente de energia é:
a) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2
b) 1s2 2s2 2p6 3s2 3p6 4s2 4p6 3d10 5s2
c) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 5s2
d) 1s2 2s2 2p6 3s2 3p6 4p6 4s2 3d10 5s2
e) 1s2 2s2 2p6 3p6 3s2 4s2 4p6 3d10 5s2
6) (OSEC) Sendo o subnível 4s1 (com um elétron) o mais energético de um átomo, podemos afirmar que:
- o número total de elétrons desse átomo é igual a 19;
- esse apresenta quatro camadas eletrônicas;
III. a sua configuração eletrônica é 1s2 2s2 2p6 3s2 3p6 3d10 4s1
a) Apenas a firmação I é correta.
b) Apenas a firmação II é correta.
c) Apenas a firmação III é correta.
d) As afirmações I e II são corretas.
e) As afirmações II e III são corretas.
7) (CESCEM) Qual dos valores abaixo pode representar o número atômico de um átomo que, no estado fundamental, apresenta apenas dois elétrons de valência?
- a) 16
- b) 17
- c) 18
- d) 19
- e) 20
1) Distribuição eletrônica no diagrama de Pauling:
a) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d4
b) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14 5s2 5p6 5d4 6s2
c) K = 2; L = 8; M = 18; N = 32 ; O = 12; P = 2
d) O subnível mais energético é sempre o último a receber elétrons no diagrama de Pauling; logo, no átomo de tungstênio esse subnível é o 5d, apresentando 4 elétrons.
e) O subnível mais externo de um átomo é sempre aquele que se encontra mais afastado do núcleo, ou seja, localiza-se na camada de valência. No tungtênio temos 6 níveis de energia; logo, o subnível mais externo está localizado no nível 6 ou na sexta camada. Assim, os elétrons mais externos estão situados no subnível 6s, contendo 2 elétrons.
Distribuição Eletrônica – Exercícios
I. seu número atômico é 25;
II. possui 7 elétrons na última camada;
III. apresenta 5 elétrons desemparelhados;
IV. pertencem a família 7A.
Estão corretas as afirmações:
a) I, II e III somente
b) I e III somente
c) II e IV somente
d) I e IV somente
e) II, III e IV somente
02. (UFSC) O número de elétrons em cada subnível do átomo estrôncio (38Sr) em ordem crescente de energia é:
a) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2
b) 1s2 2s2 2p6 3s2 3p6 4s2 4p6 3d10 5s2
c) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 5s2
d) 1s2 2s2 2p6 3s2 3p6 4p6 4s2 3d10 5s2
e) 1s2 2s2 2p6 3p6 3s2 4s2 4p6 3d10 5s2
03. (ABC) De acordo com e regra de Hund, estrutura eletrônica do átomo de carbono, no estado fundamental, é representada por:
a) 1s2 2s2 3p2
b) ![]()
c) 1s2 2s2 2p2
d) ![]()
e) ![]()
04. Conceitue orbital de um elétron.
05. Indique a distribuição eletrônica do oxigênio (Z = 8) no estado fundamental.
06. (ITA) O número máximo de orbitais atômicos correspondente ao número quântico principal é:
a) n
b) 2n
c) 2n + 1
d) n2
e) 2n2
07. (CESCEM) Qual dos valores abaixo pode representar o número atômico de um átomo que, no estado fundamental, apresenta apenas dois elétrons de valência?
a) 16
b) 17
c) 18
d) 19
e) 20
08. (PUC) O número normal de subníveis existentes no quarto nível energético dos átomos é igual a:
a) 1
b) 2
c) 3
d) 4
e) 5
09. (OSEC) Sendo o subnível 4s1 (com um elétron) o mais energético de um átomo, podemos afirmar que:
I. o número total de elétrons desse átomo é igual a 19;
II. esse apresenta quatro camadas eletrônicas;
III. a sua configuração eletrônica é 1s2 2s2 2p6 3s2 3p6 3d10 4s1
a) Apenas a firmação I é correta.
b) Apenas a firmação II é correta.
c) Apenas a firmação III é correta.
d) As afirmações I e II são corretas.
e) As afirmações II e III são corretas.
Respostas
| 01. B | 02. A | 03. B |
04. É a região de maior probabilidade para localizarmos um elétron.
05. É a região de maior probabilidade para localizarmos um elétron.
O estado fundamental é aquele em que cada elétron está na situação de menor energia permitida.
Seguindo o diagrama de Pauling, para o átomo de oxigênio, que apresenta 8 elétrons, temos: 1s2 2s2 2p4
| 06. D | 07. E | 08. D | 09. D |
Números Quânticos – Exercícios
01. (FEI) Quais são os quatro números quânticos dos dois elétrons mais externos do átomo de número atômico 20?
02. (PUC) Assinale a alternativa que não é correta:
a) O número máximo de elétrons em cada orbital é dois.
b) No nível quântico principal quatro há dois orbitais.
c) No subnível 5f há 7 orbitais.
d) Os elétrons de um mesmo átomo pode ter no máximo três números quânticos iguais.
e) 5, 1, 0 e –1/2 são quatro números quânticos do elétron de maior energia de um átomo do elemento que pertence ao grupo 1A da Tabela Periódica.
03. Analise o texto:
O número máximo de elétrons em um nível pode ser dado pela expressão 2n2, onde n é o número quântico principal do nível.
Assim, o número máximo de elétrons para o quinto nível seria, teoricamente:
a) 50
b) 32
c) 18
d) 8
e) 20
04. Analise o texto:
O número máximo de orbitais em um subnível pode ser dado pela expressão (2l + 1), onde l é o número quântico secundário.
Sendo assim, um subnível com l = 5 apresentaria:
a) 11 orbitais
b) 10 orbitais
c) 9 orbitais
d) 8 orbitais
e) 7 orbitais
05. Assinale a alternativa falsa:
a) Os números quânticos servem para identificar cada elétron de um átomo.
b) Teoricamente, um átomo apresenta infinitos níveis e infinitos subníveis de energia.
c) O quinto nível de um átomo possui 6 subníveis reais.
d) Um elétron sempre apresentará um spin quando em sua posição normal em relação ao núcleo.
e) Orbital é a região de maior probabilidade para se localizar um elétron.
Nota: Não existe convenção oficial sobre o valor do spin do primeiro elétron de um orbital.
Respostas:
01.
| n | l | m | s | |
| 1° elétron | 4 | 0 | 0 | -1/2 |
| 2° elétron | 4 | 0 | 0 | +1/2 |
Nota: Não existe convenção oficial sobre o valor do spin do primeiro elétron de um orbital.
| 02. E | 03. A | 04. A | 05. C |



